为什么是水分活度?
当人们意识到水分含量无法充分解释微生物生长波动的原因时,水活度作为质量和安全指标的实用性便得到了认可。几十年来,水活度(aw)这一概念一直为微生物学家和食品技术专家所采用。它是评估食品安全和质量最常用的指标。
水分活度:一切都与能量有关
什么是水分活度?
拿一杯水和一块干海绵。将海绵的一角浸入杯中。水会从杯中渗入海绵。
水活度是促使水渗入海绵的驱动力。为了更好地理解这一点,不妨想想海绵里的水与杯子里的水有何不同。
玻璃杯里的水是自由的,但海绵里的水却绝非如此。它受氢键、毛细力和范德华-伦敦力的束缚。这些被称为基质效应。海绵里的水处于比玻璃杯里的水更低的能量状态。水会流入海绵,但要让它流出来,我们必须通过挤压海绵来做功。
海绵中的水比玻璃杯中的水具有更低的蒸气压、更低的凝固点和更高的沸点。它们在我们可以测量和量化的方面存在差异。
水的能量也可以通过用溶质稀释水来降低。这种现象被称为渗透效应。由于需要做功才能使水恢复到纯净、自由的状态,因此这也降低了水的活度。能量的总变化是基质效应和渗透效应之和。
水分活度决定食品的质量与安全
将含水量为20%的饼干与含水量为30%的奶酪馅料混合。这会做出软塌塌的饼干吗?如果这两种原料的水活度相同,就不会。需要避免一整批香料结块吗?只要使各组分的水活度一致,问题就解决了。
维生素的降解与水分活度有关。脂质氧化、脆度、嚼劲、软度以及许多其他质量因素也是如此。水分含量只能告诉你产品中含有多少水分,仅此而已。它无法预测上述任何其他质量和安全问题。
预测安全性和稳定性
水活度可预测产品在微生物生长、化学及生化反应速率以及物理性质方面的安全性与稳定性。图1展示了产品稳定性(包括微生物生长极限和降解反应速率)与水活度之间的关系。
通过测量和控制水分活度,可以:
- 预测哪些微生物可能是导致变质和感染的潜在来源
- 保持产品的化学稳定性
- 最大限度地减少非酶褐变反应和脂质的自发自催化氧化反应
- 延长酶和维生素的活性
- 优化产品的物理特性,以改善水分迁移、质地和保质期
水分活度是如何测量的?
如果我们将样品置于密封容器中,容器顶部空间内空气的相对湿度将与样品的水活度达到平衡。在平衡状态下,两者将相等,因此我们可以通过测量顶部空间的相对湿度来确定样品的水活度。这是关于如何测量水活度这一问题最可靠的答案。
辅助方法:湿度计、电容传感器
与早期的水分活度仪类似,大多数现代仪器都采用电容式或电阻式湿度传感器来测量样品上方头空间中的湿度。
这些湿度计采用间接测量法:它们将电信号与相对湿度相关联,必须使用已知的盐标准进行校准。
只有当样品和传感器的温度相同时,这些传感器测得的ERH值才等于样品的水活度。要获得准确的测量结果,必须做好温度控制或温度测量。电容式传感器结构简单,常用于价格相对低廉的水活度仪中。
露点是一种主要方法
回答“如何测量水分活度”这一问题的最佳方法是采用p/p0比值的一级方法。P0(饱和蒸气压)仅取决于样品的温度(如附图所示),因此可以通过测量样品温度来测定P0。P(样品中水的蒸气压)可通过测量样品上方密封头空间中水的蒸气压来获得。测量该蒸气压最精确的方法,也是最符合基本原理的方法,是测量空气的露点。

“主要方法”指直接测量,无需校准
露点(或冷镜露点)法的主要优势在于速度和准确性。冷镜露点传感器是一种基于基本热力学原理的直接测量方法。冷镜水活度仪通常能在约5分钟内完成高准确性(±0.003aw)的测量。由于该测量基于温度测定,因此无需校准。 用户应测量标准盐溶液以验证仪器是否正常工作。对于某些应用,该方法的高速特性使制造商能够对产品的水分活度进行在线监测。
AQUALAB 4TE采用冷镜露点法,文献表明这是目前市场上最快、最准确的水活度测定方法。观看视频了解其工作原理。
政府法规建议使用水分活度
美国食品药品监督管理局已将水分活度纳入安全法规。这些法规详细规定了具体的要求和操作规范,以确保产品在卫生条件下生产,且纯净、健康、安全。请参考下表,了解美国政府建议采用水分活度的相关安全法规。
| 代理机构 | 产品类型 | 参考编号 | 最后更新 | 描述 |
| 美国食品药品监督管理局 | 食品 | 《食品安全现代化法案》第103条 | 2016年5月12日 | 描述了预防性措施及基于风险的安全方法,指出了监测预防性控制措施的必要性,但未具体提及水分活度 |
| 美国食品药品监督管理局 | 食品 | 《联邦法规》第21篇第117部分 | 2016年5月12日 | 概述了危害分析及基于风险的预防性控制措施的实施方法,包括针对水分活度等检测项目的监测方法(文中未特别提及水分活度) |
| 美国食品药品监督管理局 | 食品 | 2013年食品法规 | 2017 | 《食品法典》作为新《食品安全现代化法案》(FSMA)法规的一部分,为确定危害及预防性控制措施提供了指导。2017年版《食品法典》中“安全食品的时间/温度控制”章节所列出的“潜在危险食品”定义,是基于有效水活度(aw)和pH值,并采用了交互表A和B。 |
| 美国食品药品监督管理局 | 食品 | 《联邦法规》第21篇第113部分 | 2016年5月1日 | 据称,经热处理的食品若其温度低于0.85,则不易滋生细菌;但该规定属于旧版标准,已被2013年版《食品法典》中的相关内容所取代。 |
| 美国食品药品监督管理局 | 食品 | 《联邦法规》第21篇第110.8节 | 2015年4月4日 | 本节“生产操作(2)”中概述的GMP规定指出,可通过监测产品的水分活度来验证GMP的符合性,以确保其保持在安全水平 |
| 美国农业部 | RTE肉类 | 通用HACCP模型10 | 2005年5月2日 | 指出水活度是监测干燥过程的合适方法,特别是可以替代水分-蛋白质比值 |
| 美国农业部 | RTE肉类 | 肉干合规指南(含小型加工厂) | 2014年5月27日 | 指出有必要验证水分活度,以证明产品符合关键控制点的要求;建议将水分活度控制在0.70以下以抑制霉菌生长,但也提及了0.85这一数值 |
| 美国农业部 | RTE肉类 | 《李斯特菌控制合规指南》 | 1-2014 | 讨论了确保产品不含李斯特菌的各种方法,包括一种能抑制细菌生长的灭活后处理(水活度可用于此目的,但文中并未特别提及) |
| USP | 制药 | USP 922 | 2021年5月 | 本指南提供了关于水活度测定的指导及具体方法。规定了仪器确认和校准的方法。并提供了结果报告的指导。 |
| USP | 制药 | USP 51 | 2016年5月1日 | “微生物检测方法”现说明,该检测仅适用于水分活度高于0.60的产品,并引用了《美国药典》第1112条。 |
| ICH | 制药 | Q6A 决策树 6 和 8 | 1999年10月 | 如能说明该产品本身干燥,从而无法滋生微生物,并提供相关科学依据,则可能无需进行微生物限值检测 |
| ISO | 化妆品 | ISO 2961 | 2010年6月1日 | 微生物学低风险产品的风险评估与识别指南——多次提及水分活度 |
水活度简化保质期
如果没有准确、针对具体产品的保质期数据,您可能会将仍可食用但已过期的产品当作废品处理,也可能将实际上已变质但未过期的产品出售。您可能会为那些对产品毫无帮助的包装支付过高费用,或者错失因采用更优质包装而本可获得的显著保质期延长。关键在于,由于您是在“摸着石头过河”,因此无法确切知晓这些情况。
那么,为什么人们不进行更多的保质期测试呢?
通常,这是因为进行一次真正全面的保质期测试是一项艰巨的任务。它涉及水分、温度与产品失效模式之间的复杂关系。
许多因素都可能导致产品不安全或难以入口——例如发霉、微生物滋生、变质、质地或风味变化,以及维生素流失。大多数人缺乏专业知识,无法在内部进行全面的保质期测试,而委托外部实验室进行测试又成本高昂。
对于此类保质期测试,有一种科学依据充分的替代方案,即基于水分活度的简化保质期评估法。通过这种方法,只需进行一项任何人(甚至小型初创企业)都能负担得起的实验,即可获得预测产品保质期所需的所有数据。
保质期与水分活度
水分活度如何影响保质期?
- 这有助于消除干扰。一旦掌握了产品的水分活度,您就能明确哪些失效模式会对该产品造成影响。
- 这简化了保质期的预测。您可以结合水分活度仪与另一种测量方法(具体选用哪种取决于您的产品特定失效模式),在内部进行一项简便的实验,从而准确预测产品的保质期。
- 它使生产流程标准化。您可以设定水分活度指标,从而确保每批产品都能达到最佳保质期。
您的保质期数据能提供宝贵的洞察,帮助您避免产品失效、预测并延长保质期、选择最具成本效益的包装方案,以及实现更多目标。
影响保质期的因素
影响保质期的主要因素有三:微生物特性、化学变化和物理变质。这些因素都与水分活度有关。
微生物生长
微生物的生长存在一个极限水活度值,低于该值它们便无法生长。决定微生物生长所需“有效”水下限的是水活度,而非水分含量。由于细菌、酵母和霉菌需要一定量的“有效”水来维持生长,因此将产品设计为水活度低于临界值,是控制微生物生长的有效手段。
产品中可能含有水分,甚至含量很高,但如果其能量水平足够低,微生物就无法利用这些水分来维持生长。这种“沙漠般”的条件会在微生物与当地环境之间造成渗透失衡。因此,微生物无法生长。
霉菌和微生物的滋生是影响保质期的最大威胁。控制水分活度可以抑制或阻止微生物滋生,延长保质期,并使某些产品无需冷藏即可安全储存。通过使用明确的表格,您可以为产品设定水分活度限值,并在保质期测试中加以应用。
| 啊 | 细菌 | 霉菌 | 酵母 | 典型产品 |
| 0.97 | 肉毒杆菌 E 荧光假单胞菌 | 新鲜肉类、水果、 蔬菜、罐装水果、罐装蔬菜 | ||
| 0.95 | 大肠杆菌 产气荚膜梭菌 沙门氏菌属 霍乱弧菌 | 低盐培根、熟香肠、 鼻喷雾剂、眼药水 | ||
| 0.94 | 肉毒杆菌A型、B型 副溶血性弧菌 | 黑曲霉 | ||
| 0.93 | 蜡样芽孢杆菌 | 黑毛霉 | 一些奶酪、腌制肉类(火腿) 烘焙食品, 炼乳,ral 液体 悬浮液、外用乳液 | |
| 0.92 | 单核细胞增生李斯特菌 | |||
| 0.91 | 枯草芽孢杆菌 | |||
| 0.90 | 金黄色葡萄球菌 (厌氧) | 玫瑰毛孢菌 | 酿酒酵母 酿酒酵母 | |
| 0.88 | 念珠菌 | |||
| 0.87 | 金黄色葡萄球菌 (需氧菌) | |||
| 0.85 | 棍状曲霉 | 加糖炼乳、陈年奶酪(切达奶酪)、发酵香肠(萨拉米香肠)、肉干、培根、大多数浓缩果汁、巧克力糖浆、水果蛋糕、软糖、止咳糖浆、口服镇痛混悬液 | ||
| 0.84 | 白丝蛾 | |||
| 0.83 | Penicillium expansum 岛青霉 青霉属(Penicillium viridicatum) | 汉氏德哈里莫斯 | ||
| 0.82 | 烟曲霉 寄生曲霉 | |||
| 0.81 | 青霉属 青霉属(Penicillium cyclopium) 扁平青霉 | |||
| 0.80 | 拜氏酿酒酵母 | |||
| 0.79 | 马氏青霉 | |||
| 0.78 | 黄曲霉 | 果酱、橘子酱、杏仁糖、糖渍水果、糖蜜、干无花果、咸鱼 | ||
| 0.77 | 黑曲霉 黄曲霉 | |||
| 0.75 | 限制型曲霉 白色曲霉 | |||
| 0.71 | 欧蒂姆·谢瓦利耶 | |||
| 0.70 | 阿姆斯特丹欧蒂姆 | |||
| 0.62 | 鲁氏酿酒酵母 | 果干、玉米糖浆、甘草、棉花糖、口香糖、宠物干粮 | ||
| 0.61 | 双孢红曲菌 | |||
| 0.60 | 无微生物繁殖 | |||
| 0.50 | 无微生物繁殖 | 焦糖、太妃糖、蜂蜜、面条、外用软膏 | ||
| 0.40 | 无微生物繁殖 | 全蛋粉、可可粉、液心止咳糖 | ||
| 0.30 | 无微生物繁殖 | 饼干、淀粉类零食、蛋糕预拌粉、维生素片、栓剂 | ||
| 0.20 | 无微生物繁殖 | 硬糖、奶粉、婴儿配方奶粉 |
化学降解
水分活度会影响导致食品变质的化学反应速率,因为水既可作为溶剂,本身也可作为反应物,或通过粘度改变反应物的迁移性。 例如,非酶褐变反应随水活度的增加而增强,在0.6至0.7 aw时达到峰值;而脂质氧化则在约0.2至0.3aw时降至最低。根据吸湿等温线测定,最佳化学稳定性通常出现在单分子层含水率附近。
身体状况恶化
高湿度和(较少见的)低湿度环境会影响产品的水分活度,导致产品质地或物理性质发生不良变化,并缩短保质期。常见问题包括:干性产品失去酥脆感、粉末结块、湿性产品口感发硬或嚼劲过强。确定产品的临界水分活度可能需要进行一些研究,但水分活度这一指标能让这一过程变得更加简单。

包装、运输和仓储
运输和储存过程中水分活度的变化会显著影响保质期。水分活度与温度密切相关,而运输和储存温度会影响包装内的水分活度。简化的保质期测试可帮助您确定最佳包装方案,并评估运输和储存条件对产品保质期的影响。
等温线精准定位水活度的最佳区间
预测产品随时间推移的变化
食品制造商需要了解产品在发霉、变软、变质、变酸、结块、结疙瘩、结晶以及不再被消费者接受之前,还能保存多长时间。吸湿等温线是预测和延长产品保质期的有力工具。它能帮助您:
等温线:配方研发的圣杯
水分吸附等温线是一幅图表,显示了在恒定温度下,随着水分被产品吸附和脱附,水分活度(aw)如何变化。这种关系非常复杂,且每种产品都有其独特性。 水分活度几乎总是随着水分含量的增加而升高,但这种关系并非线性。事实上,大多数食品的吸湿等温线呈S形(S型曲线),而含有结晶物质或高脂肪含量的食品则呈J形。
手工制作的方法不切实际
绘制等温线的经典方法是将样品置于装有水活度已知的盐溶液的干燥器中,直至样品重量不再变化。随后称量样品,以测定其含水量。每个样品在等温线曲线上对应一个数据点。
由于该过程耗时较长,传统上通常使用五到六个数据点,结合GAB或BET等曲线拟合方程来构建曲线。
一种更快捷的等温线绘制方法
手动绘制吸湿等温线是一项费时费力的工作。 该方法亟需实现自动化。最初采用的方法——至今仍被大多数蒸汽吸附仪所采用——被称为DVS,即动态蒸汽吸附法。在该方法中,样品暴露于湿度受控的气流中,同时微天平会测量样品在吸附或脱附水分时产生的微小重量变化。一旦达到平衡,仪器便会动态地切换到下一个预设的湿度水平。测试时间从两天到数周不等。
DVS法在研究吸附动力学方面效果显著——即产品在接触特定湿度时会发生什么变化,以及其吸附或脱附水分的速度如何。然而,DVS法在绘制高分辨率等温线时并不十分有效,因为每个平衡步骤在等温线上仅产生一个数据点。
DDI等温线揭示了前所未见的景象
动态露点等温线(DDI)法正是为解决这一问题而设计的。该方法通过在样品暴露于加湿或干燥空气时,每5秒对水分活度和含水量进行一次采样,从而生成高分辨率等温线,清晰呈现吸附和脱附曲线的细节。 DDI图包含数百个数据点,并揭示了此前无法观察到的细节,例如发生结块、结团、潮解以及质地丧失的关键点。
等温线是如何生成的
AQUALAB VSA可自动生成快速、高分辨率的 DDI 和 DVS 等温线图,彻底改变您对产品的认知。双重测试模式与先进的建模软件将您的数据转化为解决方案,助您制造、监测、储存和运输优质产品。
将等温线数据转化为解决方案
VSA 配备了直观且功能齐全的建模软件。水分分析工具包将向您展示如何利用经过研究验证的预测模型,将数据转化为解决方案。您可以在一个易于使用的程序中找到所需的所有模型。 识别玻璃化转变的关键湿度、评估包装性能、测定吸湿性、追踪滞后现象、预测涂层失效、判断易结块/结团倾向,以及更多功能。
等温线确定了临界水分活度值
尽管采用了双层包装并制定了严格的储存温度指南,一家喷雾干燥奶粉生产商仍面临结块问题。
当玻璃化转变成为问题时
当牛奶经过喷雾干燥时,快速蒸发会使糖分处于玻璃态。玻璃态乳糖与结晶态乳糖的性质截然不同。由于粒子移动性低,粉末处于玻璃态时,粒子不会结块或聚集成团。结晶结构属于低能态,因此总会有部分分子处于从玻璃态向结晶态的过渡过程中。当这种过渡速率达到临界点时,问题便会出现。
水活度可预测转变速率
当水活度(aw)为0.30时,所有乳糖可能需要数年时间才能结晶;当水活度为0.40时,可能只需一个月;而当水活度超过0.43时,这一转变将在数小时内发生。一旦乳糖结晶,奶粉就会发生永久性变化。其吸水能力会发生剧烈变化,无法溶解,且口感也会变差。简而言之,它已经变质了。
DDI等温线可预测玻璃化转变点

对于喷雾干燥奶粉等粉末,可通过高分辨率DDI等温线测定其玻璃化转变点。传统的等温线依赖于模型来填补测量点之间的间隙。DDI等温线可测量数百个数据点,并能识别诸如喷雾干燥奶粉的玻璃化转变点等相变现象。
等温线二阶导数曲线的峰值表明,临界相变值为0.43aw。
通过在生产线上进行常规、准确的检测并采用更优的控制值,该制造商成功提高了出货合格率。
创建混合模型
某蛋糕制造商正在研制一款夹心蛋糕的配方。该配方的组成包括糖霜(含水量约7%)、奶油馅(12%)和蛋糕体(15%)。此前,在保质期内发生的水分迁移曾导致质地问题,例如蛋糕变干、糖霜变硬,以及液化的奶油馅渗入蛋糕体。
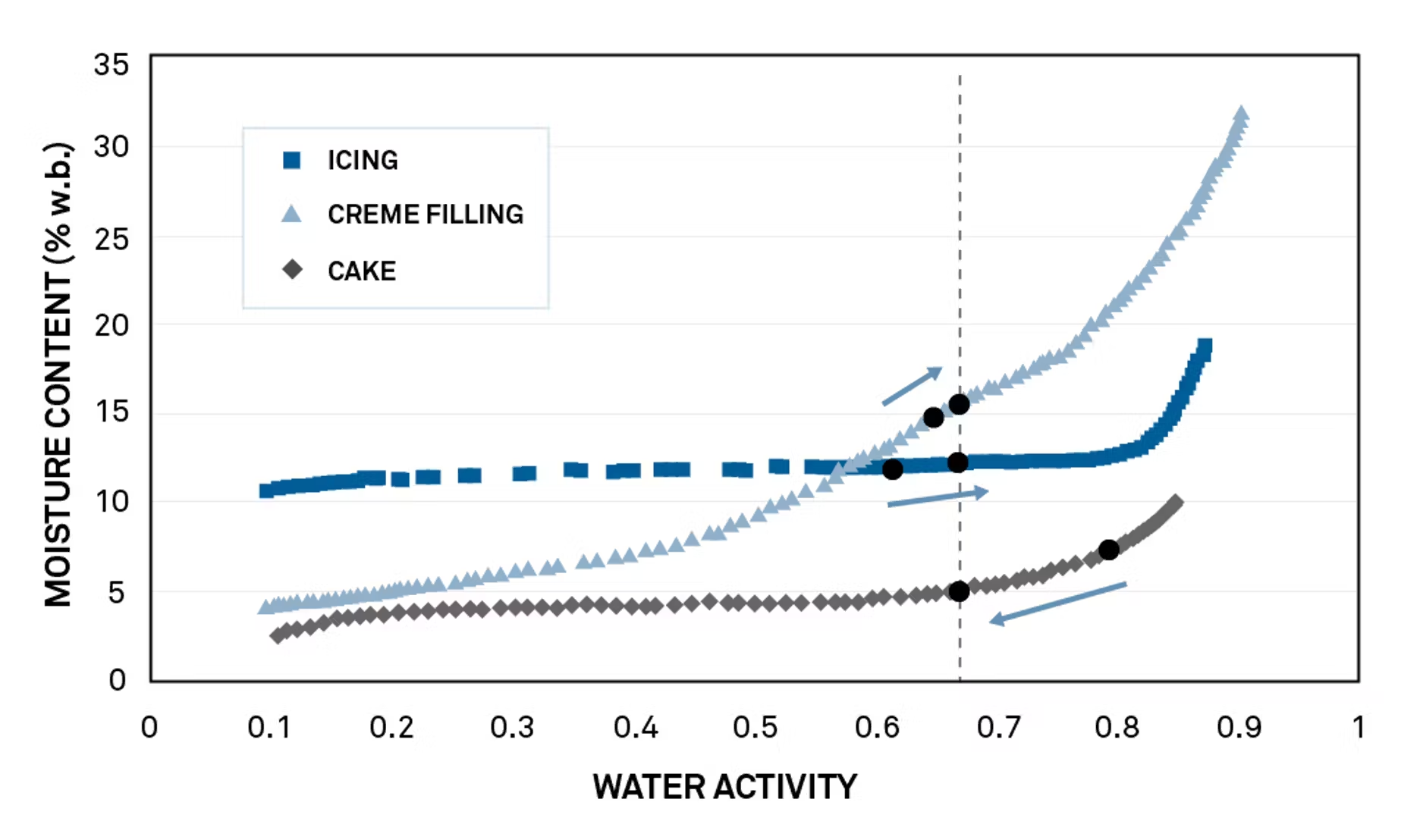
了解水分在组件之间如何流动
各配料的吸湿等温线显示,糖霜(最干燥的配料)的水活度最高,为0.79。奶油和蛋糕的水活度相近,分别为0.66和0.61。
预测最终产品的水分活度
将等温线转换为chi图后,预测最终产品的水分活度为0.67,这对蛋糕而言是一个微生物安全的数值。
避免意外情况
随后,蛋糕师成功地在平衡水分活度(0.67)下烘焙并品尝了这款蛋糕。
选择包装
单份装粉末饮料混合剂是一个正在增长的市场细分领域。包装成本占该产品原材料成本的50%以上。包装的主要目的是在产品的目标保质期内, 将饮料混合剂的相对湿度(aw) 维持在临界值以下。
包装计算始于一个关键水分活度值。能够从动态露点等温线(DDI)中精确确定该点,使得此类包装计算成为可能。
该曲线显示了某款饮料配方玻璃化转变点的分布:
该饮料粉的关键水分活度——即确切的转折点——在25°C时为0.618。

计算包线电导率
我们利用简化的包装计算方法(可在《等温线基础》中查阅,也可作为软件工具使用),对这款饮料粉的四种不同包装进行了评估——包括其原包装和三种可能的替代方案。在高湿度条件下(25°C,75%湿度),结果如下:
了解配方变更
某宠物食品公司调整了配方,推出了一款通过水分活度控制的无防腐剂产品。产品上市不久后,便因变质问题开始出现退货。
初步评估表明,变质预测是基于在异常低的温度(15℃)下进行的水分活度测试得出的。在15℃、25℃和40℃下测得的等温线显示,如果在不当条件下储存(宠物食品往往如此),则极有可能发生变质。

等温线提供了完整的预测图景,使客户能够通过新的配方来解决问题。
调查产品故障
在连续13个种植季未出现任何问题后,一位山核桃种植户的作物因霉变问题被拒收。为此,研究人员绘制了一张等温线图以调查该问题。
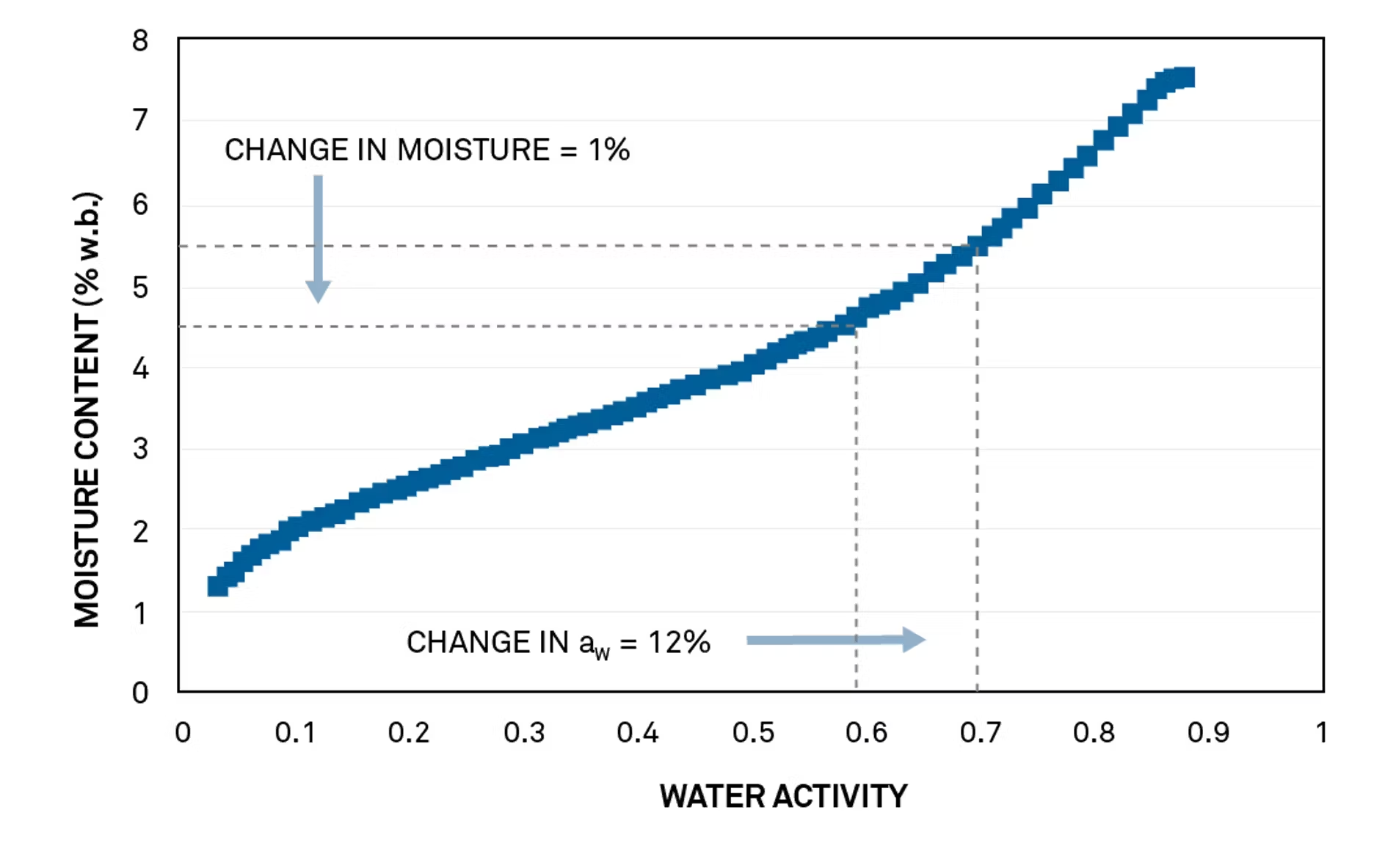
为了防止微生物滋生,山核桃必须干燥至0.60aw。如等温线所示,0.60aw对应的山核桃含水率为4.8%。此外,山核桃的等温线在此关键控制区域内相当平缓,因此含水率的微小变化会导致水活度的显著且潜在危险的变化。
等温线显示设定值过低
完整的等温线图表明,该山核桃种植者的加工流程不足以保证其农产品的安全与质量。该种植者通过干燥减重法测定水分含量。由于其出厂标准为5%,且测量准确性为±0.5%,因此干燥后农产品的实际水分含量可能在4.5%至5.5%之间。
无论是高湿度环境下的储存,还是包装不当,都可能导致山核桃吸收过多的水分,从而变质。
采用动态露点等温线(DDI)的研究
Allan, Matthew 和 Lisa J. Mauer. “单晶成分及混合物潮解点测定方法的比较.” 《食品化学》195 (2016): 29-38. doi:10.1016/j.foodchem.2015.05.042.
Allan, Matthew, Lynne S. Taylor 和 Lisa J. Mauer. “共离子效应对结晶性配料混合物潮解点降低的影响。”《食品化学》195 (2016): 2-10. doi:10.1016/j.foodchem.2015.04.063.
巴里(Barry)、丹尼尔·M.(Daniel M.)和约翰·W.·巴西克(John W. Bassick)。《NASA航天飞机先进乘员逃生服的研发》。SAE技术论文集,1995年。doi:10.4271/951545。
Bonner, Ian J., David N. Thompson, Farzaneh Teymouri, Timothy Campbell, Bryan Bals 和 Jaya Shankar Tumuluru. “序贯氨纤维膨胀(AFEX)预处理和制粒对玉米秸秆吸湿性能的影响。”《干燥技术》第33卷,第14期(2015):1768-778。doi:10.1080/07373937.2015.1039127。
卡特(B.P.)、加洛韦(M.T.)、坎贝尔(G.S.)和卡特(A.H.),2016。《基于动态露点等温线分析谷物在临界水分活度下的透湿性变化》。《美国农业与生物工程师学会学报》,59(3):1023-1028。
卡特(B.P.)、加洛韦(M.T.)、莫里斯(C.F.)、韦弗(G.L.)和卡特(A.H.),2015。《将水分活度作为小麦调质和面粉生产技术指标的依据》。《谷物食品世界》60(4):166-170。
卡特(Carter),布雷迪·P.;玛丽·T. 加洛韦(Mary T. Galloway);盖隆·S. 坎贝尔(Gaylon S. Campbell);以及阿伦·H. 卡特(Arron H. Carter)。《基于动态露点等温线的临界水分活度作为低水分饼干酥脆度的指标》。《食品测量与表征杂志》第9卷第3期(2015年):463-70页。 doi:10.1007/s11694-015-9254-3.
卡特(Carter, Brady P.)、玛丽·T·加洛韦(Mary T. Galloway)、盖隆·S·坎贝尔(Gaylon S. Campbell)和阿伦·H·卡特(Arron H. Carter)。《基于动态露点等温线的临界水分活度作为预混粉稳定性的指标》。《食品测量与表征杂志》第9卷第4期(2015年):479-86页。 doi:10.1007/s11694-015-9256-1.
卡特(B.P. Carter)与施密特(S.J. Schmidt). 2012. 利用水分吸附等温线测定食品玻璃化转变的最新进展. 《食品化学》132:1693-1698.
Coronel-Aguilera, Claudia P.,及 M. Fernanda San Martín-González。《利用流化床包衣技术对喷雾干燥的β-胡萝卜素乳液进行包衣》。《LWT——食品科学与技术》第62卷第1期(2015年):187-93页。 doi:10.1016/j.lwt.2014.12.036.
Fonteles、Thatyane Vidal、Ana Karoline Ferreira Leite、Ana Raquel Araújo Silva、Alessandra Pinheiro Góes Carneiro、Emilio De Castro Miguel、Benildo Sousa Cavada、Fabiano André Narciso Fernandes 及 Sueli Rodrigues。 “利用超声处理促进腰果苹果渣浆的干燥:对抗氧化特性及生物活性化合物体外生物利用度的影响。”《超声学与声化学》31 (2016): 237-49. doi:10.1016/j.ultsonch.2016.01.003.
郝、法义、卢丽新和王军。《储存过程中多组分食品水分迁移的有限元分析》。《食品加工工程学报》第40卷第1期(2016年)。doi:10.1111/jfpe.12319。
郝、法义、卢丽新和王军。《不同储存条件下透气包装中对湿气敏感的饼干保质期预测的有限元模拟》。《食品加工与保鲜》第40卷第1期(2015年):37-47页。doi:10.1111/jfpp.12581。
Kuang, Pengqun, Hongchao Zhang, Poonam R. Bajaj, Qipeng Yuan, Juming Tang, Shulin Chen, and Shyam S. Sablani. "利用麦芽糊精和蔗糖经喷雾干燥法制备的叶黄素微胶囊的理化性质及贮存稳定性." 《食品科学杂志》第80卷第2期(2015年)。 doi:10.1111/1750-3841.12776.
刘伟、王海峰、顾西凤、全灿、戴新华。《酒石酸钠二水合物和柠檬酸钾一水合物标准物质含水量的认证》。《分析方法》第8卷第13期(2016年):2845-851。doi:10.1039/c5ay03067f。
Marquez-Rios, E., V.m. Ocaño-Higuera, A.n. Maeda-Martínez, M.e. Lugo-Sánchez, M.g. Carvallo-Ruiz 及 R. Pacheco-Aguilar。 “柠檬酸作为太平洋狮爪扇贝(Nodipecten subnodosus)肉干燥的预处理。”《食品化学》第112卷,第3期(2009年):599-603页。doi:10.1016/j.foodchem.2008.06.015。
Penner, Elizabeth A. 与 Shelly J. Schmidt. “采用新型蒸汽吸附分析仪测得的水分吸附等温线与标准饱和盐浆法测得结果的比较.”《食品测量与表征》第7卷第4期(2013年):185-93页。 doi:10.1007/s11694-013-9154-3.
Rao, Qinchun, Mary Catherine Fisher, Mufan Guo 和 Theodore P. Labuza. “商业化鸡蛋蛋黄粉在干燥及中等含水率食品基质中的贮存稳定性。”《农业与食品化学杂志》第61卷,第36期(2013年):8676-686。 doi:10.1021/jf402631y.
Rao, Qinchun, Andre Klaassen Kamdar, Mufan Guo 和 Theodore P. Labuza. “牛酪蛋白及其水解物对蛋白质面团模型系统在储存期间硬化现象的影响.” 《食品控制》60 (2016): 621-28. doi:10.1016/j.foodcont.2015.09.007.
Syamaladevi、Roopesh M.、Ravi Kiran Tadapaneni、Jie Xu、Rossana Villa-Rojas、Juming Tang、Brady Carter、Shyam Sablani 和 Bradley Marks。《高温条件下通用小麦粉和花生酱中沙门氏菌的水活度变化及其热稳定性》。《国际食品研究》81 (2016): 163-70。 doi:10.1016/j.foodres.2016.01.008.
魏美琳、王晓翔、孙静静、段先英。《基于Ni(II)离子和2,2′-联吡啶-3,3′-二羧酸的3D POM–MOF复合材料:晶体结构与质子电导率》。 《固态化学杂志》202 (2013): 200-06. doi:10.1016/j.jssc.2013.03.041.
魏ML,孙JJ,王XJ. “掺杂金属-席夫碱-POM-MOF的硅酸盐凝胶复合材料的制备及质子电导率评价.”《溶胶-凝胶科学与技术》71卷第2期(2014):324-28. doi:10.1007/s10971-014-3370-0.
Yuan, X., Carter, B.P. 和 Schmidt, S.J. 2011. 利用自动水蒸气吸附仪测定聚葡萄糖发生玻璃态向橡胶态转变的临界相对湿度。《食品科学杂志》,76(1): E78-89.
Zabalaga, Rosa F., Carla I.a. La Fuente, 及 Carmen C. Tadini. “对未成熟香蕉片(Musa cavendishii)在对流干燥过程中的热物理性质的实验测定。”《食品工程学报》187 (2016): 62-69. doi:10.1016/j.jfoodeng.2016.04.020.
附录:
水活度与含水率
人们通常认为水活度比水分含量更难测量。但要获得准确且可重复的水分含量测量结果,其实并没有表面上看起来那么简单。
理论上,水分含量的测定很简单。只需测定产品中的水分含量,并将其与产品中其他成分的重量进行比较即可。但实际上,要准确测定产品中的水分百分比,却是一个困难且复杂的过程。原因如下。
不同的报告方法会引起混淆
水分含量通常以湿基或干基表示。对于湿基,水分含量等于水含量除以样品总重量(固体部分加上水分)。对于干基,水分含量等于水含量除以干重(仅固体部分)。 遗憾的是,水分含量通常仅以百分比形式报告,且未注明采用何种方法测定。虽然湿基与干基之间的换算较为简单,但在比较基于不同基准报告的水分含量时,仍会产生混淆并引发潜在问题。此外,以干基报告的水分含量实际上可能导致百分比值超过100%,从而造成更大的混淆。
测量方法各异,导致无法进行比较
AOAC列出了35种不同的水分测定方法。这些方法分为直接测定法和间接测定法两类。直接测定法是指先从样品中去除水分(通过干燥、蒸馏、萃取等方式),然后通过称重或滴定来测定水分含量。直接测定法能提供最可靠的结果,但通常耗时且费力。 具体方法包括空气烘箱干燥、真空烘箱干燥、冷冻干燥、蒸馏法、卡尔·费歇尔法、热重分析法、化学干燥法以及气相色谱法。
间接法不会从样品中去除水分,而是通过测量随水分含量变化而变化的某种食品特性来进行测定。这些方法需要参照一种主要方法或直接法进行校准,其准确度受主要方法准确度的限制。 间接法通常速度快且样品制备要求低,但可靠性不如直接测量法。间接测量法的例子包括折光法、红外吸收法、近红外吸收法、微波吸收法、介电电容法、电导率法和超声吸收法。
测量含水率的过程还因以下因素而变得更加复杂:一种测量方法得出的结果未必与其他方法一致,而且含水率数值通常不会注明所采用的测量方法。
即使是直接测量方法,也无法提供一致的结果。任何需要加热样品的方法(即干燥减量法)都可能导致有机挥发物的损失或样品的分解(特别是对于含糖量较高的样品)。 例如,如果样品中存在有机挥发物,或者样品在干燥过程中发生分解,那么不受挥发物损失或分解影响的卡尔·费歇尔分析法所得结果将与干燥减量分析法不同。
变化是难以避免的
解决这些问题的办法之一,就是采用统一的方法,并且只比较通过相同方法获得的数值。遗憾的是,即使在水分含量分析中保持测量方法的一致性,也无法彻底消除所有问题。例如,考虑一下干燥减量法。这种方法看似相当简单。 先称量样品并记录其重量,随后将样品转移至烘箱中干燥,最后测量其干重。通过将初始重量减去干重来确定含水量,然后根据报告方法的不同,将含水量计算为含水量除以干重或总重。
即便是这种简单的干燥减量法,也暗藏着诸多潜在的变异性陷阱。最根本的问题在于,“干燥”一词并无真正的科学含义,且从未被明确界定。因此,必须针对每个样品建立一个可重复的、任意的干燥标准。“干燥”通常被定义为重量损失停止的时刻。然而,热重分析曲线显示,不同产品的重量损失在不同温度下趋于平稳。 此外,根据产品的不同,“干燥”所需的时间也会有所差异,且对一种产品能达到“干燥”的温度,对另一种产品可能导致分解。 这意味着每个样品都有其独特的理想烘箱温度和干燥时间。对于某些产品,文献中提供了这种理想的时间/温度组合,但对于许多产品则没有相关数据。对于未经测试的产品,很难确定应采用哪种组合。如果未使用相同的时间/温度组合,则不应比较所得的含水量。
另一个问题是,许多烤箱即使设定为同一温度,实际温度随时间推移也可能与设定值相差多达15 °C;而两台设定为相同温度的烤箱,其实际温度差异甚至可能高达40 °C。
仅就干燥减量法而言,其额外的变异来源包括:烘箱蒸气压、样品制备方法、样品粒度、样品称量以及干燥后的处理。有趣的是,尽管存在这些潜在的陷阱,但当文献中报告了通过干燥减量法测得的含水率时,人们往往会立即将其视为正确值。 此外,在对各种含水率测定方法进行比较时,若其中一种方法是干燥减量法,人们总是默认干燥减量法的测量结果是正确的。
什么是“干”?
明确“干燥”的定义有助于消除水分测量中的一些不一致性。定义“干燥”的最佳方法是确定一种烘箱干燥状态下的水分活度。 此时,干重即指样品达到该烘箱干燥水活度时的重量。在25 °C和30%相对湿度的常见环境条件下,假设烘箱内的蒸汽压与外界空气相同,将烘箱温度设定为95 °C可在箱内形成0.01 aw的烘箱干燥水活度。 无论环境条件如何,只要能维持烘箱内水活度恒定为0.01 aw,该烘箱便能创造出科学意义上的“干燥”条件。在此类烘箱中,当任何产品的重量停止变化时,即可判定其为干燥状态。此时其水活度为0.01 aw,其重量即为干重。 只要将烘箱内的水分活度维持在0.01 aw,即可通过调节烘箱的蒸汽压和温度来防止挥发性物质的释放。采用此方法可消除因多种测量方法及“干燥”定义不明确而导致的不一致性。
更精确的水分分析
水分含量能提供有关产量和数量的宝贵信息,因此从经济角度来看至关重要。它还能反映产品的质地,因为水分含量的增加会提高产品的流动性并降低玻璃化转变温度。但要获得准确且一致的水分含量数值往往颇具难度,而且如果不了解测定方法,仅凭水分含量数值本身是无法得出可靠结论的。 当产品中的水分含量被用来描述其实际并不具备的特性(如产品质地、质量或微生物安全性)时,还会引发其他问题。在这些及其他情况下,水分活度才是更准确的测量指标。为了进行全面的水分分析,食品和药品研发人员应同时测量水分含量和水分活度。此外,还可以利用水分吸附等温线来确定并维持最佳的保质期、质地、安全性和质量。
水活度的科学定义
水活度源于热力学和物理化学的基本原理。作为一项热力学原理,定义水活度时必须满足以下要求:纯水(aw = 1.0)为标准状态,系统处于平衡状态,且温度已明确规定。
在平衡状态下
μ = μo + RT ln (f/fo)
其中:μ(J mol⁻¹) 是系统的化学势,即每摩尔物质的热力学活度或能量;μ₀是纯物质在温度T(°K) 下的化学势;R为气体常数(8.314 J mol⁻¹ K⁻¹);f为物质的逸度或逸出倾向;fo为纯物质的逸出倾向(van den Berg 和 Bruin,1981)。某物质的活度定义为a = f/fo。在涉及水时,需为该物质标注下标
aw= f/fo
aw 是水的活度,即系统中水的逸出倾向除以无曲率半径的纯水的逸出倾向。在实际应用中,对于食品所处的绝大多数条件而言,逸度可近似视为蒸气压(f ≈ p),因此
aw = f/fo ≅ p/po
当系统各处的μ值相同时,系统便达到平衡。液相与气相之间的平衡意味着这两个相中的μ值相同。正是这一事实使得通过测量气相来确定样品的水活度成为可能。
水活度定义为材料中水的蒸气压(p)与同温度下纯水的蒸气压(po)之比。 空气的相对湿度定义为空气蒸气压与其饱和蒸气压之比。当达到蒸气-温度平衡时,样品的水活度等于密封测量室中包围样品的空气的相对湿度。将水活度乘以100即可得到平衡相对湿度(ERH),单位为百分比。
aw = p/po = ERH (%) / 100
水活度是衡量系统中水能量状态的指标。有几个因素会影响系统中的水活度:
- 溶质(如盐或糖)的渗透作用是通过偶极-偶极相互作用、离子作用和氢键与水相互作用的
- 毛细现象:由于水分子间氢键发生变化,弯曲液面(液面凸起)上方水蒸气的压强小于纯水的蒸气压
- 表面相互作用是指水通过偶极-偶极力、离子键(HO 或 OH)、范德华力(疏水键)以及氢键,与未溶解成分(如淀粉和蛋白质)上的官能团直接相互作用3–
正是这三种因素在食品中的综合作用,降低了水的能量,从而使相对湿度低于纯水。这些因素可大致分为两类:渗透效应和基质效应。
由于渗透作用和基质相互作用程度各异,水活度描述了系统中水所处的能量状态连续体。水在不同程度上受到力的“束缚”。这是一种能量状态的连续体,而非静态的“束缚”状态。 水活度有时被定义为系统中的“自由水”、“结合水”或“有效水”。尽管这些术语更易于理解,但它们未能充分阐明水活度概念的各个方面。
水活度受温度影响。温度会通过改变水的结合状态、水的解离、溶质在水中的溶解度或基质状态来改变水活度。尽管溶质的溶解度可能是一个控制因素,但通常主要受基质状态的控制。由于基质状态(玻璃态与橡胶态)取决于温度,因此温度会影响食品的水活度也就不足为奇了。 温度对食品水分活度的影响因产品而异。有些产品的水分活度随温度升高而增加,有些则随温度升高而降低,而大多数高水分食品的水分活度随温度变化微乎其微。因此,甚至无法预测水分活度随温度变化的方向,因为这取决于温度如何影响食品中控制水分活度的各项因素。
作为一种潜在能量的度量,它是推动水分从高水分活度区域向低水分活度区域移动的驱动力。 水活度的这一动态特性在以下方面有所体现:多相食品(如饼干芝士三明治)中的水分迁移、水分从土壤向植物叶片的转移,以及细胞膨压。由于微生物细胞是由半透膜包围的高浓度溶质体系,水对自由能产生的渗透效应对于确定微生物的水关系及其生长速率至关重要。
一种适用于质量保证/质量控制及配方开发的强力检测方法
水分活度是衡量产品中水能量的热力学指标。贵公司为何需要掌握水分活度的测定方法?因为它与食品的微生物易感性直接相关,同时也与导致食品保质期缩短的许多反应存在直接关联。由于其测量采用具有已知标准的量表,因此特别适合作为安全和质量的规格指标。
常见问题
测定水分活度需要多长时间?
像 AQUALAB 4TE 这样的现代露点仪能在约五分钟内测得水分活度值,准确性为 ±0.003 aw;电容式传感器虽然速度更快,但需要定期参照基准方法进行校准。五分钟的测试时间已足够短,足以支持在大多数生产速率下进行生产过程中的质量检查。
如何降低食品中的水分活度?
通过添加保湿剂(如盐、糖、甘油或丙二醇)来降低水分活度,这些成分能结合水分子并降低其蒸气压;也可通过从产品中去除水分,或结合这两种方法来实现。吸附等温线能反映配方中的每项调整如何影响最终的水分活度,因此对于在不需反复试验的情况下达到目标水分活度(aw)至关重要。
水活度的阈值是多少?超过该阈值,食品就需要冷藏吗?
美国食品药品监督管理局(FDA)将水活度(aw)高于0.85的产品归类为“安全温度控制(TCS)”食品,这意味着必须通过冷藏来确保其安全性。水活度在0.85及以下的产品通常被认为能有效抑制病原菌的生长,保持货架稳定性,但即使在水活度低至0.70时,仍存在霉菌滋生的风险。
两种单独使用时安全的成分,混合后会变得不安全吗?
是的,如果它们的水活度不同,水分会从水活度较高的组分向水活度较低的组分迁移,直到达到平衡;而最终达到平衡后的水活度可能高到足以支持病原体的生长。在混合组分之前先使它们的水活度一致,可以避免这种水分迁移的风险。
水活度可以在生产车间测量吗,还是必须在实验室进行?
台式水分活度仪专为生产环境设计,无需在实验室中使用——AQUALAB 4TE 广泛应用于食品制造工厂的生产线上。此外,还提供在线传感器选项,可在加工过程中进行连续监测,无需逐样取样。
订阅电子报
您一定会喜欢的案例研究、网络研讨会和文章。
定期获取最新内容!

