Webinare
Warum sich Pulver schlecht benehmen
Verklumpen, Verklumpen, Verfestigen bei der Lagerung, Anhaftungen an Maschinen – wenn Sie mit Pulvern arbeiten, kennen Sie die offensichtlichen Probleme und Fehlverhalten.
Aber vielleicht haben Sie noch nicht gesehen, welche gefährlichen Schäden Pulver an anderer Stelle anrichten kann. Diese weniger sichtbaren, weniger bekannten Probleme können schwerwiegende Folgen haben – wie Gesundheitsrisiken und Produktrückrufe. Ignorieren Sie sie auf eigene Gefahr.
Begleiten Sie Mary Galloway, Leiterin des METER Food R&D Lab, und Dr. Zachary Cartwright, leitender Lebensmittelwissenschaftler, bei der Vorstellung neuer Forschungsergebnisse und der Erläuterung der vielen Gründe, warum Pulver sich unvorhersehbar verhalten.
Sie lernen:
- Wie viele Unternehmen stellen die funktionellen Vorteile ihrer Produkte versehentlich falsch dar?
- Die mikrobiellen Risiken von Lebensmitteln mit geringem Feuchtigkeitsgehalt und die gefährlichen Irrtümer darüber
- Die Vielzahl der Faktoren, die die Pulverstabilität beeinflussen, und welche davon am wichtigsten zu beachten sind
- Wie man genau feststellt, wo Pulverprobleme auftreten werden, und wie man sie verhindert, bevor sie entstehen
Über die Moderatoren
Mary Galloway ist Leiterin des METER Food Research & Development Lab. Sie ist spezialisiert auf die Verwendung und Prüfung von Instrumenten, die die Wasseraktivität und deren Einfluss auf physikalische Eigenschaften messen. Sie hat mit Dutzenden der weltweit größten und erfolgreichsten Lebensmittelmarken zusammengearbeitet, um Probleme mit Produkten im Zusammenhang mit Feuchtigkeit zu lösen.
Dr. Zachary Cartwright ist leitender Lebensmittelwissenschaftler bei der METER Group. Er hat einen Doktortitel in Lebensmittelwissenschaft von der Washington State University und einen Bachelor-Abschluss in Biochemie von der New Mexico State University. Er ist Experte für Isothermanalysen und den Einsatz des Vapor Sorption Analyzer (VSA).

Transkript, zur besseren Verständlichkeit bearbeitet
Zachary:
Hallo zusammen. Willkommen bei „Why Powders Misbehave“. Mein Name ist Zachary Cartwright.
Mary:
Und ich bin Mary Galloway.
Zachary:
Beginnen wir mit einem kurzen Überblick darüber, was Sie heute erwartet. Wir werden darüber sprechen, was Pulver sind, versuchen, Ihnen eine Definition zu geben, und uns dann hauptsächlich auf drei verschiedene Aspekte von Pulvern konzentrieren. Wir werden uns mit der physikalischen Stabilität wie Verklumpung und Verlust der Fließfähigkeit befassen. Mary hat einige Labordaten, die sie uns vorstellen wird, und dann werden wir uns mit der chemischen Stabilität befassen und über Ranzigkeit oder Bräunungsreaktionen nachdenken. Ich glaube, Sie haben auch einige Forschungsergebnisse für uns.
Mary:
Ja, das tue ich. Wir haben im Labor eine Studie zum Abbau von Vitamin C durchgeführt.
Zachary:
Abschließend werden wir uns noch mit der mikrobiellen Stabilität befassen. Auch wenn es sich um eine Umgebung mit geringer Wasseraktivität handelt, gibt es dennoch einige mikrobiologische Bedenken, und ich glaube, Sie haben gerade an einem Artikel gearbeitet oder wurden in einem Artikel zitiert, auf den wir uns konzentrieren werden.
Pulver 101: Grundlagen und Definitionen
Zachary:
Mary, was ist ein Puder? Wie würdest du einen Puder definieren?
Mary:
Nun, die meisten Menschen wissen theoretisch, was ein Pulver ist, da wir es an so vielen Orten finden. Als wir zuvor darüber gesprochen haben, war der Markt von Bedeutung. Als wir über die Kategorie der Pulver gesprochen haben, konnten wir Gewürze und Zutaten nennen. Die Pharmaindustrie verwendet den Begriff auch für Hilfsstoffe und Wirkstoffe, die viele verschiedene Funktionen erfüllen.
Grundsätzlich ist ein Pulver ein kleines körniges Produkt. Wir haben eine gute Definition in einem Artikel von Bandari aus dem Jahr 2017 gefunden. Um es mit anderen Worten zu sagen: Darin wird die Struktur als Hauptmerkmal eines Pulvers beschrieben. Amorph, kristallin oder eine Kombination aus beidem. Die Wechselwirkung zwischen diesen beiden Eigenschaften und die Partikelgröße beeinflussen die Funktionalität, die Anwendung und die Herstellung des Pulvers.
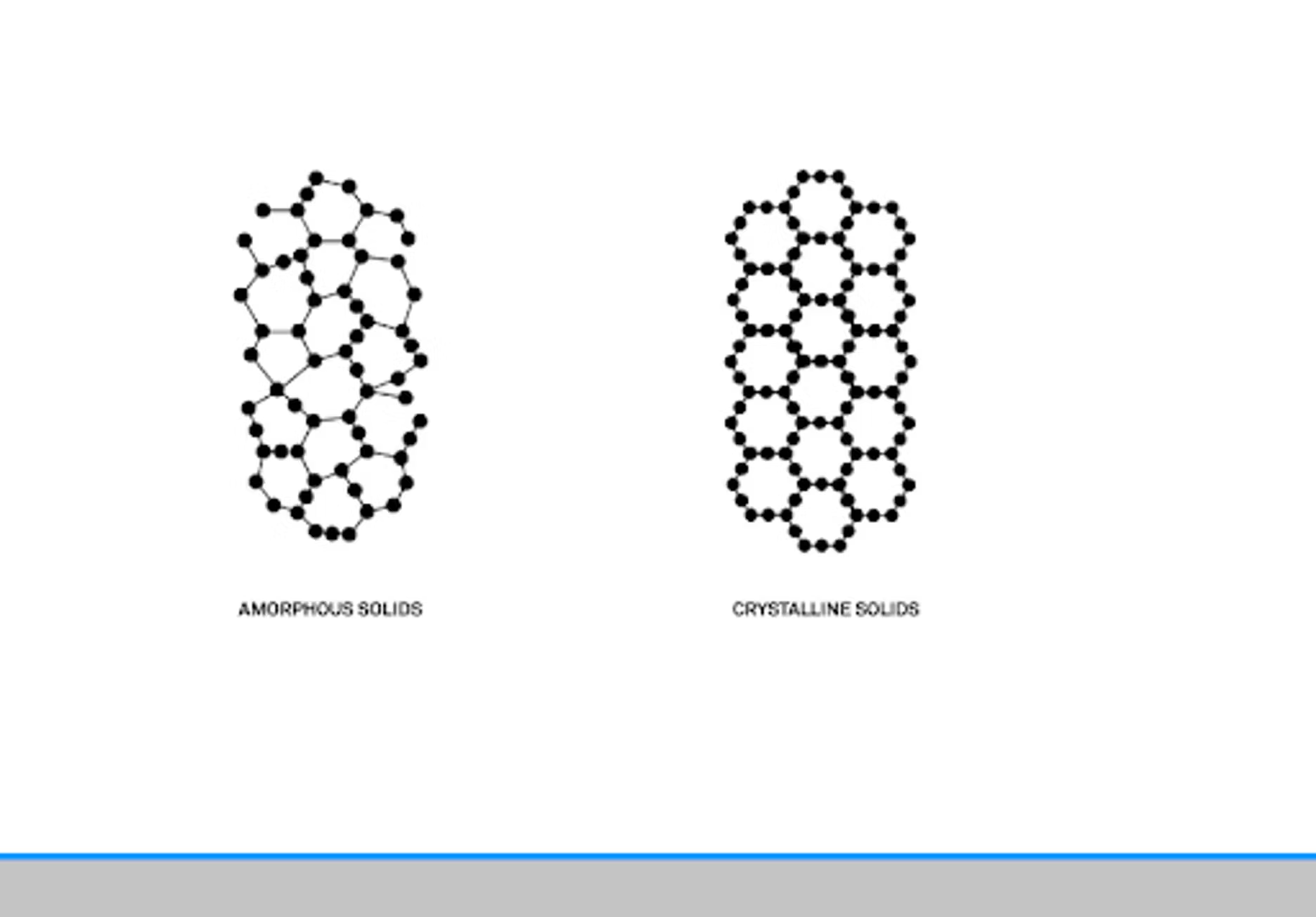
Das erklärt, warum Pulver einen so großen Markt darstellen und warum sie so schwierig sind – weil sie so viele verschiedene Märkte und Funktionsgruppen umfassen.
Zachary:
Wir haben bereits ein Webinar zum Thema Pulver durchgeführt, in dem wir uns etwas eingehender mit amorphen und kristallinen Pulvern befasst haben. Grundsätzlich gibt es einige wesentliche Unterschiede in der Molekülstruktur. Eine kristalline Struktur weist eine sich wiederholende, klar definierte Struktur auf. Das lässt sich auf molekularer Ebene erkennen. Selbst mit bloßem Auge lassen sich diese Unterschiede bei Pulvern erkennen, und wir haben dazu einige Abbildungen.
Letztes Mal haben wir über das Mischen dieser Pulver gesprochen und uns einige der kombinierten Effekte angesehen. Wenn Sie sich näher damit befassen möchten, können Sie sich unser vorheriges Webinar noch einmal ansehen. Wir haben auch über die Partikelgröße gesprochen, und darauf möchte ich noch einmal näher eingehen. Wie wirkt sich die Partikelgröße auf einige Eigenschaften von Pulvern aus?
Mary:
Die Partikelgröße hat einen großen Einfluss auf die Eigenschaften von Pulvern und ist der Grund, warum diese so schwierig sein können. Bei kleinen Partikelgrößen kann es zu unerwarteten Brückenbildungen zwischen den Partikeln kommen, wodurch diese klebrig werden und agglomerieren können.
Neben der allgemeinen Partikelgröße gibt es noch einige andere Faktoren. Auch die Partikelform spielt eine Rolle. Es gibt auch einige Forschungsergebnisse, die zeigen, dass beim Mischen kristalliner Pulver ein Phänomen auftritt, das wir als Delikveszenz bezeichnen. Dabei geht das Material früher als erwartet von einem festen in einen flüssigen Zustand über, als dies bei den einzelnen Pulvern zu erwarten wäre. Der Grund dafür sind die unterschiedlichen Partikelgrößen.
Wann immer es zu solchen Kontaktstellen kommt, kann es zu Brückenbildung und Problemen kommen. Kristalline Pulver können besonders schwierig sein, da sie, wie Sie sagten, eine sehr geordnete Struktur haben, was bedeutet, dass die Feuchtigkeit im Wesentlichen nur an der Außenseite der Struktur haftet. Im Gegensatz zu einem amorphen Pulver handelt es sich nur um eine Oberflächeninteraktion, da es viele Spalten und unregelmäßige Formen und Größen gibt und Wasser sich leichter mit dem amorphen Pulver verbinden kann. Das macht sie zwar funktional unterschiedlich, hat aber auch Auswirkungen, wenn Sie sie als Formulierer verwenden müssen.
Zachary: Als wir das letzte Mal miteinander gesprochen haben, haben wir uns die fünf Phasen der Verklumpung angesehen. Es gibt mehrere Schritte, um zur Agglomeration und schließlich zur Verflüssigung zu gelangen.
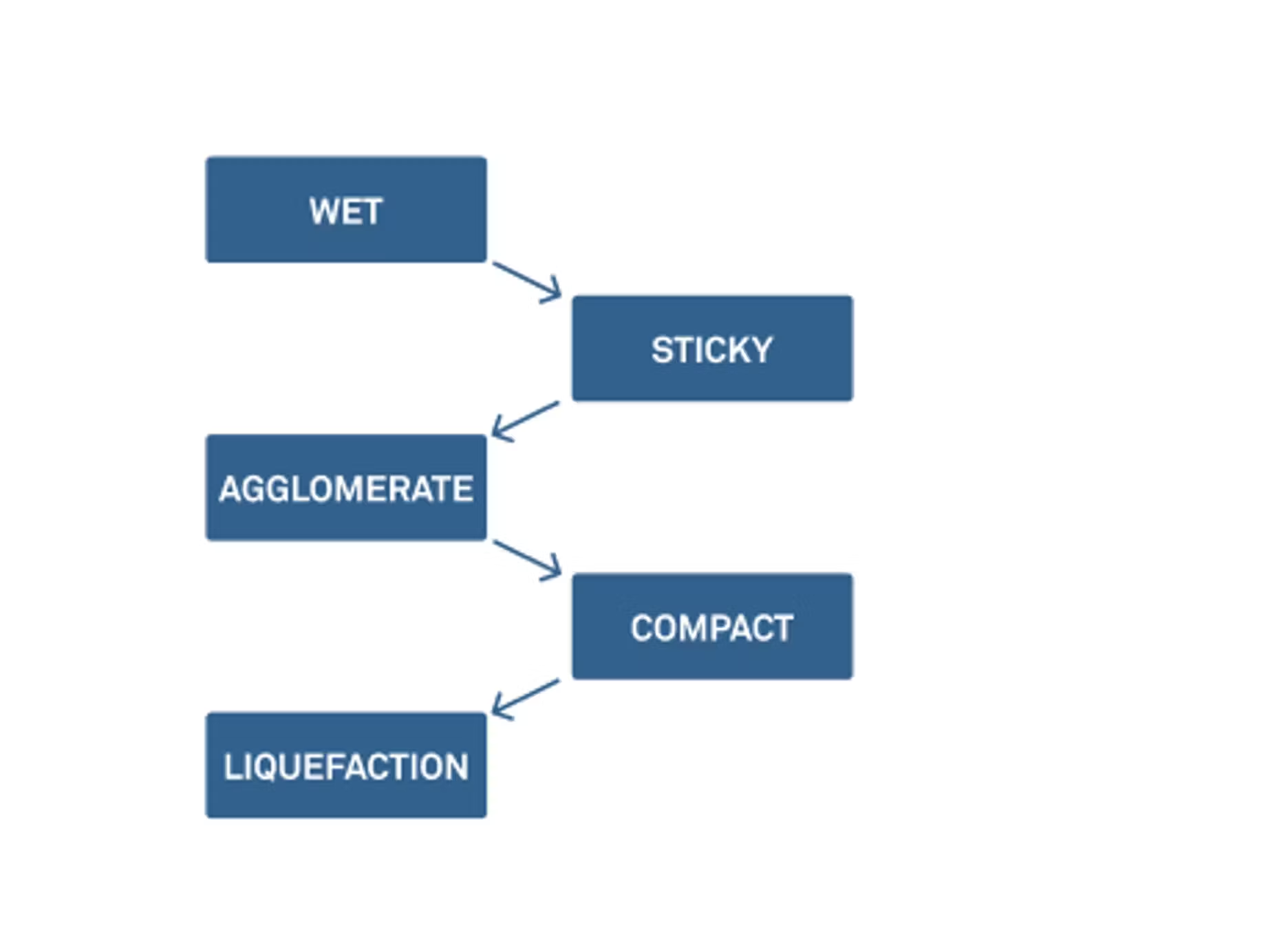
Wir müssen das heute nicht unbedingt durchgehen, aber ich möchte darauf hinweisen, dass es schon in einem frühen Stadium zu Verklumpungen und Verbackungen kommen kann. Eine Möglichkeit, dies zu kontrollieren, besteht darin, die Feuchtigkeit und die Wasseraktivität dieser Pulver zu betrachten. Wir tun dies in den meisten unserer Webinare, aber es ist immer hilfreich, zu definieren, was Feuchtigkeitsgehalt und Wasseraktivität sind, und darüber zu sprechen, wie wir diese Dinge zusammen nutzen können, um über physikalische Veränderungen und chemische und mikrobielle Stabilität nachzudenken.
Beginnen wir mit dem Feuchtigkeitsgehalt und der Wasseraktivität. Ich weiß, dass Sie dazu eine sehr anschauliche Grafik und eine gute Definition haben. Wie unterscheiden Sie diese beiden Messgrößen voneinander?
Mary:
Für einige unserer Gesprächspartner ist die Wasseraktivität ein neues Konzept, während die meisten Menschen mit dem Feuchtigkeitsgehalt bestens vertraut sind. Ich trenne diese beiden Begriffe gerne voneinander und sage, dass es zwei Arten der Wassermessung gibt. Bei der einen betrachten wir die Wassermenge oder den Feuchtigkeitsgehalt. Bei der anderen betrachten wir die Energie des Wassers – was kann das Wasser bewirken? Diese beiden Werte messen wir auf völlig unterschiedliche Weise.
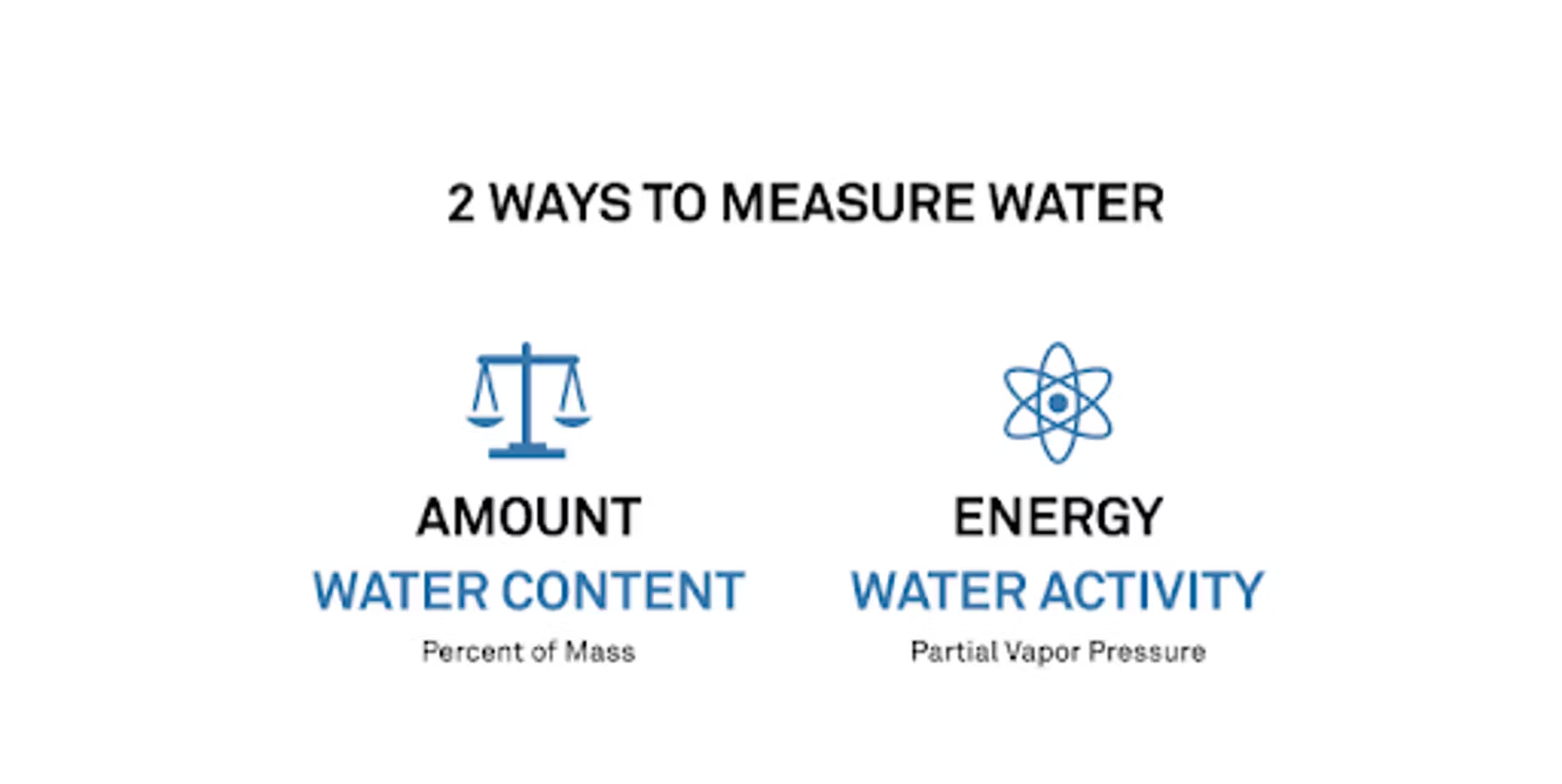
Wenn wir den Feuchtigkeitsgehalt betrachten, handelt es sich um einen Massenanteil, wir betrachten also lediglich das Gewicht. Wenn wir jedoch die Wasseraktivität betrachten, messen wir eigentlich das, was wir als Dampfdruck bezeichnen, also ähnlich wie die Feuchtigkeit, die aus einer Probe austritt.
Wenn Sie sich einige unserer Forschungsergebnisse und andere Webinare ansehen möchten, sprechen wir dort über die Wasseraktivität. Es könnte hilfreich sein, sich vor Augen zu halten, dass wir uns im Grunde genommen auf die ausgeglichene Feuchtigkeit beziehen, die die Probe abgibt. Das könnte dabei helfen, diese beiden Dinge besser zu verstehen. Auch wie sich bestimmte äußere und Umgebungsbedingungen auf Ihr Produkt auswirken können, ist etwas, das Sie beachten und beobachten sollten.
Zachary:
Guter Punkt. Ich sehe immer noch ziemlich oft, dass Wasseraktivität fälschlicherweise mit Wasserverfügbarkeit gleichgesetzt wird, und das ist nicht ganz richtig. Wasseraktivität ist ein thermodynamisches Prinzip. Es handelt sich dabei tatsächlich um die Energie dieses Wassers, und das ist wichtig zu wissen, da die Energie des Wassers für chemische Reaktionen, Texturveränderungen oder andere Vorgänge genutzt werden kann. Es ist gut, diesen Punkt zu verdeutlichen. Bei der Wasseraktivität betrachten wir die Energie des Wassers.
Wir haben Kunden, die regelmäßig zu uns kommen und über gute Werte für den Feuchtigkeitsgehalt verfügen, aber große Schwierigkeiten haben, genaue Messungen zu erhalten. Da sie den Feuchtigkeitsgehalt nicht genau bestimmen können, ist es schwierig, einige der Probleme, mit denen sie zu kämpfen haben, mit dem Feuchtigkeitsgehalt in Verbindung zu bringen. Der Feuchtigkeitsgehalt allein liefert Ihnen nicht alle Informationen, die Sie benötigen, insbesondere bei Pulvern.
Durch die Kombination von Wasseraktivität und Feuchtigkeitsgehalt können wir die Isotherme betrachten, worüber wir immer viel sprechen, aber das liegt daran, dass dies eine einzigartige Möglichkeit ist, das Wasser in diesen Produkten zu betrachten und ein vollständiges Bild davon zu erhalten, wie sich das Wasser in diesem Produkt verhält. Wie misst man eine Isotherme? Wie betrachtet man diese Form und setzt sie in Beziehung zu verschiedenen Eigenschaften eines Pulvers?
Mary:
Eine der Anwendungsmöglichkeiten von Isothermen ist die Definition eines kritischen Punktes, einer kritischen Wasseraktivität, ab der wir Texturveränderungen und andere Veränderungen innerhalb der Struktur des Produkts beobachten können. Im Grunde genommen geht es darum, ab welchem Punkt beginnt sich das Produkt zu verändern und nimmt es viel mehr Feuchtigkeit auf? Bei Pulvern ist dies in der Regel der Punkt, an dem es zu Verklumpungen und Verbackungen kommt. Bei anderen Produkten wie Snacks kann es zu einer Erweichung kommen, daher ist es wichtig, diese kritischen Punkte zu ermitteln. Wir können auch die Steigung oder die Form der Isotherme selbst betrachten und so die Struktur identifizieren, wie wir es bei amorphen und kristallinen Stoffen besprochen haben. Das können wir uns ansehen. Wir können diese Proben auch feuchter Luft aussetzen und im Grunde genommen in Echtzeit beobachten, wie sie sich verhalten. So erhalten wir viele wertvolle Informationen über das Produkt, die für einen Kunden nützlich sein können.
Zachary:
Es ist wichtig zu erwähnen, dass wir über eine einzigartige Methode namens dynamische Taupunktisotherme verfügen, die sich am besten eignet, um ein hochauflösendes Diagramm oder Bild des Wasserverhaltens zu erhalten. Es gibt noch andere Methoden, auf die wir später eingehen werden, aber die Verwendung dieser dynamischen Taupunktisotherme und des Dampfabsorptionsanalysators ist die beste Methode, um das Wasser zu charakterisieren und dann einige der Faktoren zu betrachten, die wir berücksichtigen werden, beginnend mit der physikalischen Stabilität. Im nächsten Abschnitt sprechen wir über physikalische Stabilität und was das für Pulver bedeutet.
Mary:
In Ordnung.
Charakterisierung der physikalischen Stabilität von Pulvern
Zachary:
Lassen Sie uns tiefer in die physikalische Stabilität eintauchen. Wenn wir über physikalische Stabilität und Pulver nachdenken, gibt es drei wichtige Faktoren, die wir berücksichtigen sollten: Feuchtigkeit, Temperatur und Zeit. Ich werde Sie sich damit befassen lassen und bei Bedarf weitere Informationen hinzufügen.
Mary:
Was die Feuchtigkeit betrifft, so gilt grundsätzlich: Je mehr Feuchtigkeit verfügbar ist, desto mehr Prozesse müssen verändert werden, desto mehr Strukturen müssen verändert werden. Als Sie über die DDI sprachen, dachte ich zunächst an sprühgetrocknetes Milchpulver, bei dem wir von einem glasartigen Zustand zu einem gummiartigen Zustand übergehen.
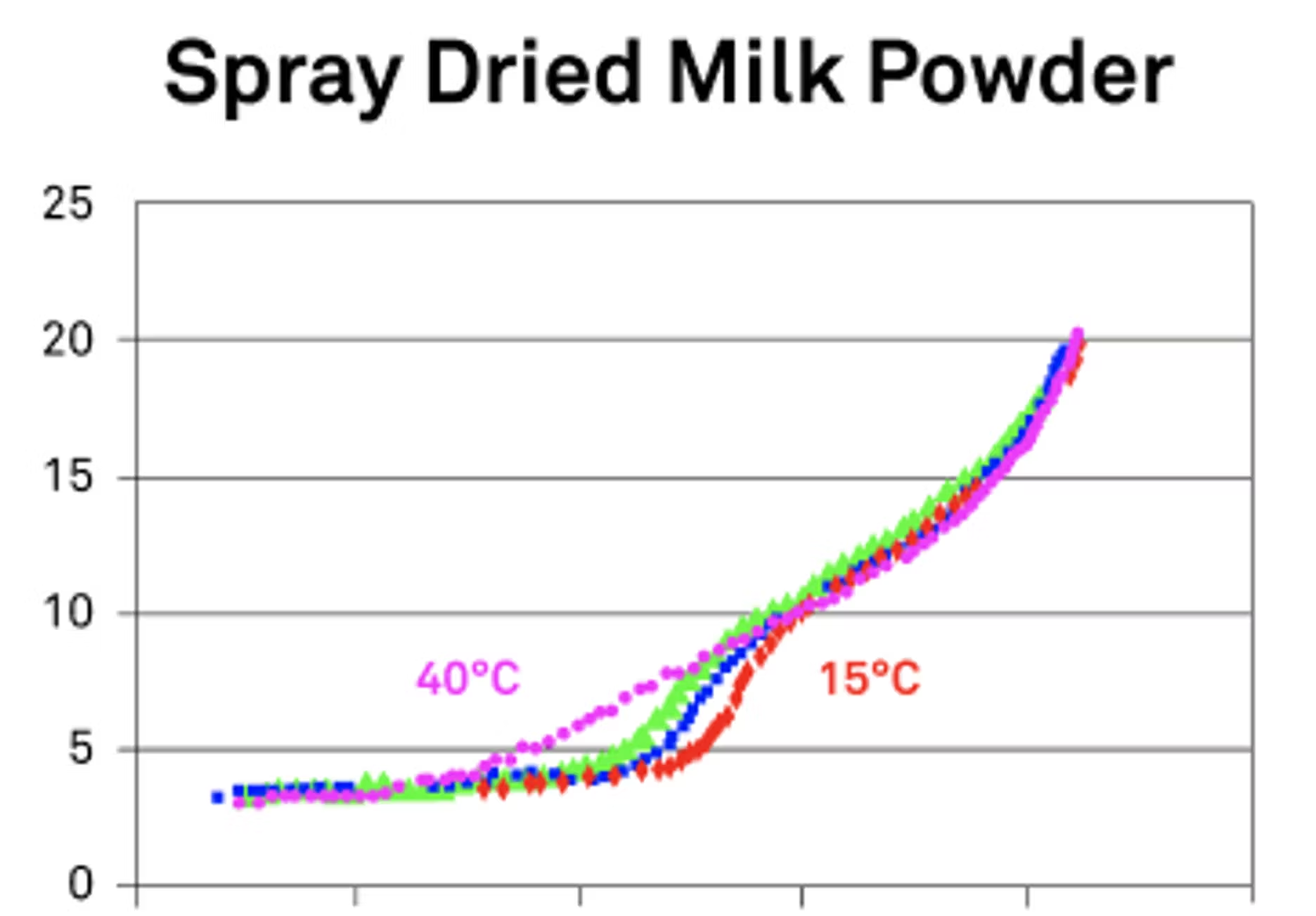
Wenn wir nun eine andere, traditionellere Art der Isotherme verwenden würden, würde man diesen Übergang tatsächlich verpassen, da er im Wesentlichen übersprungen wird. Normalerweise hält man Dinge bei einer bestimmten Luftfeuchtigkeit und beobachtet, was passiert. Aber beim DDI handelt es sich um einen Echtzeitprozess, und man kann diese Übergänge tatsächlich sehen. Das meine ich konkret, wenn ich davon spreche, Isothermen zu verwenden, um Ihre Echtzeitdaten zu sehen und zu erkennen, wann diese kritischen Punkte eintreten. Feuchtigkeit hat einen großen Einfluss auf diese Prozesse, da Wasser dazu neigt, die Vorgänge zu beschleunigen.
Es kann ein Lösungsmittel sein, es kann ein Reaktionspartner sein, und es kann sogar als Puffer in chemischen Reaktionen fungieren. Manchmal ändern sich die Rollen im Laufe des Prozesses oder wenn dem Prozess mehr Feuchtigkeit hinzugefügt wird, und dann kann man beobachten, wie sich die Reaktionsgeschwindigkeiten tatsächlich verändern. Neben der Feuchtigkeit wollen wir auch die Temperatur betrachten. Wir haben eine Grafik, die wir gerne zeigen, weil sie sehr gut veranschaulicht, wie sich der von uns erwähnte kritische Punkt verändert, wenn wir einem Produkt Wärme zuführen oder die Temperatur erhöhen. Was passiert, und das ist auch logisch, wenn man darüber nachdenkt, ist, dass diese Veränderung schneller vonstattengeht. Man fügt dem System Energie zu, und dieses System fließt schneller. Diese Veränderungen treten bei geringerer Wasseraktivität oder schneller in diesem Prozess auf.
Das Letzte ist die Zeit. Wenn man einem Prozess genügend Zeit gibt, wird er sich verändern. Selbst wenn man die anderen Faktoren wie Temperatur und Feuchtigkeit konstant halten könnte, würde dies bei ausreichender Zeit dennoch geschehen. Ich habe neulich gerade über dieses Beispiel nachgedacht. Man hat alte Glasfenster, und wenn man die Ober- und Unterseite sehr alter Glasfenster misst, würde man feststellen, dass die Unterseite dicker ist als die Oberseite, und das liegt daran, dass sie viel Zeit hatten, sich zu verflüssigen. Das ist die Idee, dass etwas, wenn man ihm genügend Zeit gibt, irgendwann zu Ende geht. Alle drei Faktoren spielen eine Rolle für die physikalische Stabilität.
Zachary:
Es ist auch wichtig zu beachten, dass es je nach Ihrer Frage verschiedene Methoden oder verschiedene Arten von Isothermen gibt, die Sie verwenden können. Zurück zur dynamischen Taupunkt-Isotherme: Mit dieser können Sie den kritischen Punkt ermitteln und genau verstehen, bei welcher Wasseraktivität oder bei welcher Kombination aus relativer Luftfeuchtigkeit und Temperatur dieser Effekt auftritt. Sobald Sie wissen, wo dieser kritische Punkt liegt, können Sie auch einen DVS-Test durchführen, einen dynamischen Dampfabsorptionstest, um die Frage nach der Zeit zu klären.
Um auf Ihr Fensterbeispiel zurückzukommen: Wie lange dauert es, bis dieser kritische Punkt unter bestimmten Bedingungen tatsächlich erreicht ist? Wir haben eine Möglichkeit, diese Frage zu beantworten. Wir verfügen über einen Dampfabsorptionsanalysator, mit dem Sie beide Methoden anwenden können. Dieses Gerät ist einzigartig und tatsächlich das einzige Instrument, das beide Methoden ausführen kann. Wenn Sie ein Problem mit der physikalischen Stabilität haben, kann es sinnvoll sein, auf beide Testarten zurückgreifen zu können.
Kommen wir nun zu Ihrem Projekt zum Mischen von Gewürzen. Was war das für ein Projekt? Was war das Ziel und was haben Sie daraus gelernt?
Mary:
Wie wir wissen, bewegt sich Feuchtigkeit aufgrund von Unterschieden in der Wasseraktivität. Die Frage ist, wie stark sie sich bewegt. Können wir das vorhersagen und wie genau ist diese Vorhersage? Wir haben ein Werkzeug dafür. Es gibt definitiv Gleichungen, die versuchen, diese Wechselwirkung zwischen Produkten zu modellieren. Für unser Projekt habe ich im Wesentlichen sechs verschiedene Mischungen genommen, einige Gewürze, einige mit Maltodextrin in Sorbit, Maisstärke und Zwiebelsalz, und dann einige Gewürze, Salbei, Oregano und Kreuzkümmel. Wir haben sie zusammengemischt. Zunächst haben wir alle Zutaten auf eine ganz bestimmte Wasseraktivität gebracht. Dann haben wir auch Isothermen für alle diese Zutaten durchgeführt, da dies ein wichtiger Faktor ist, nicht nur die anfängliche Wasseraktivität oder das Massenverhältnis im Blut, sondern auch die Eigenschaften dieser Isotherme, wie sie sich in Gegenwart von Feuchtigkeit verhält.
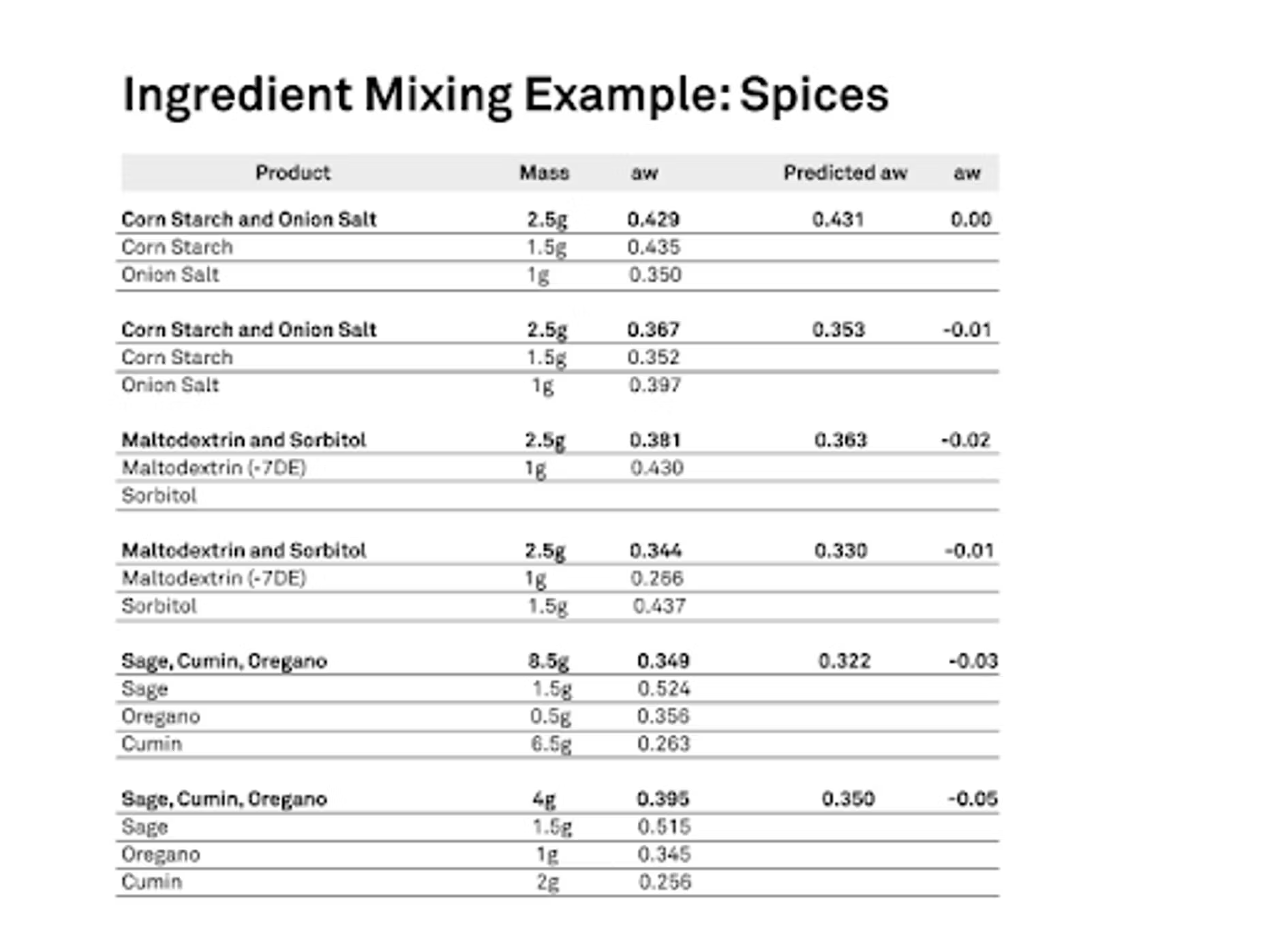
Wir möchten wissen, wie sie aufgenommen werden oder nicht, oder wie auch immer das sein mag. Wir müssen diese Informationen für dieses Produkt kennen, damit wir ein gutes Vorhersagemodell erstellen können. Wir haben dies getan und sie dann in bekannten Massenverhältnissen miteinander vermischt. Anschließend haben wir gemessen, um genau zu sehen, wie hoch die Wasseraktivität war, nachdem wir ihnen Zeit zum Ausgleich gegeben hatten. Dann haben wir auch die Vorhersage getroffen, und sie waren sehr gut. Im Grunde zeige ich die Kombinationen, die wir gemacht haben, die oberste dort, Maisstärke und Zwiebelsalz. Wir haben eineinhalb Gramm Maisstärke gemischt, und die Wasseraktivität lag zu Beginn bei 0,435. Das Zwiebelsalz haben wir mit einem Gramm gemischt, aber es hatte eine geringere Wasseraktivität. Sie sehen dort, dass die Wasseraktivität bei 0,35 begann, und dann haben wir dies gemischt, und die tatsächliche Wasseraktivität unserer Mischung betrug 0,429.
Als wir das Vorhersagemodell unter Berücksichtigung der Isothermen, der Anfangsmasse und der anfänglichen Wasseraktivitäten durchführten, sagten wir tatsächlich eine endgültige Wasseraktivität von 0,431 voraus, also ein extrem nahes Ergebnis. Diese funktionierten gut. Sie haben tatsächlich eine feine Partikelgröße, sodass sie viele Kontaktpunkte haben und man schneller ein Gleichgewicht erreicht. Das war keine große Überraschung, aber es war schön, dass es so gut funktionierte. An einigen unserer anderen Beispiele können Sie sehen, dass wir sehr gute Ergebnisse erzielt haben. Wir haben auch Maltodextrin und Sorbitol getestet. Wir haben die Mengen variiert und den Ausgangspunkt verändert. Eine war höher als die andere, und dann haben wir sie getauscht. Wir haben verschiedene Kombinationen ausprobiert, um es ein wenig zu testen. Dann haben wir auch die Gewürze am Boden getestet: Salbei, Kreuzkümmel und Oregano.
Das hat recht gut funktioniert. Unser schlimmster Fall in der Konfiguration war das allerletzte Beispiel. – Vielleicht sollte ich das nicht sagen, aber der Wissenschaftler in mir sagt mir, dass ich es tun muss. Sie werden sehen, dass unsere Vorhersage eine Wasseraktivität von 0,35 betrug, während der tatsächliche Wert bei 0,395 lag. Er war also um etwa 0,05 niedriger. Ich wollte nur kurz erläutern, wie das funktioniert, und dann zu den von uns durchgeführten Vergleichen kommen.
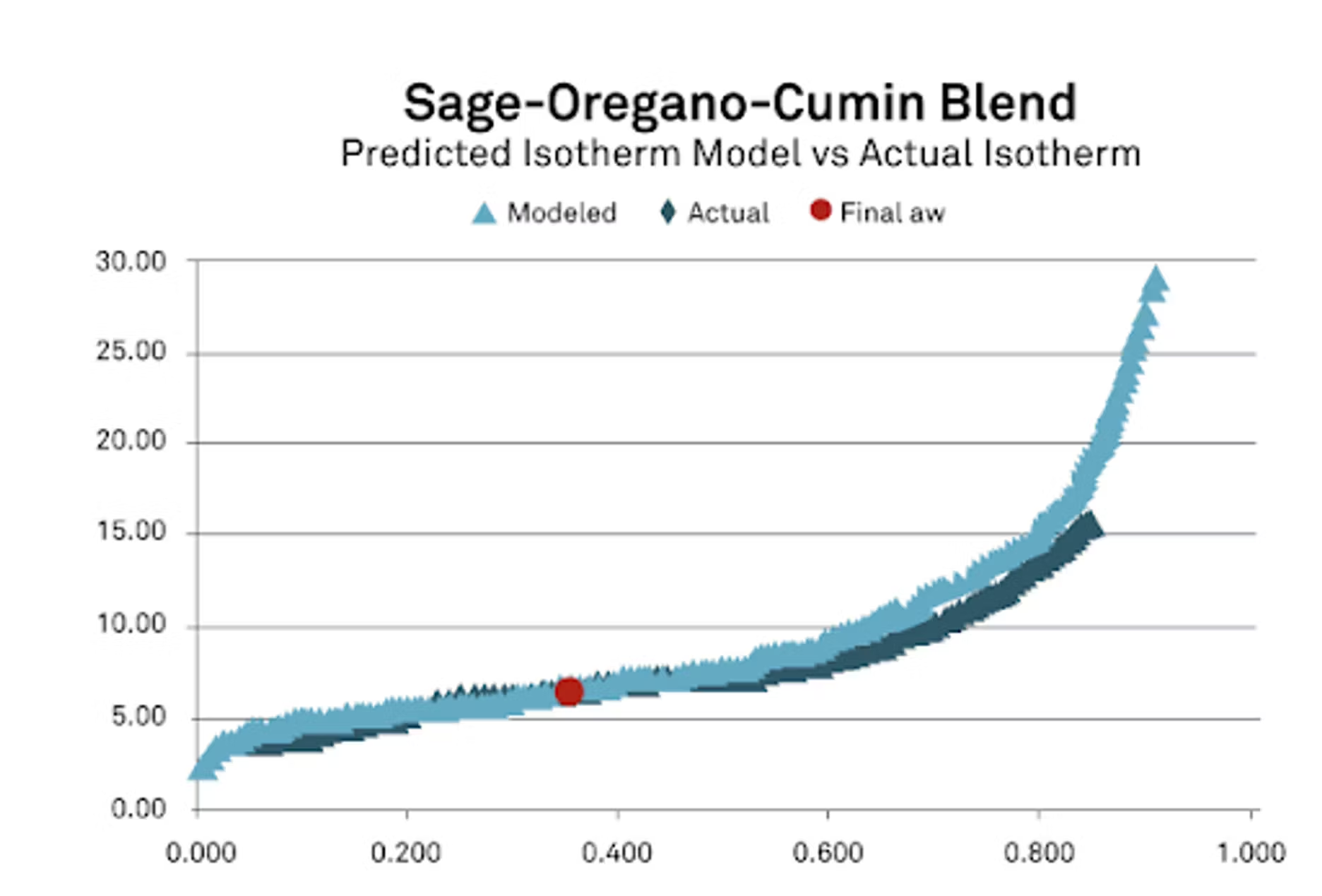
Hier sehen Sie alle Isothermen für Salbei, Kreuzkümmel, Oregano und ein kombiniertes Modell, also eine Zusammenstellung aller drei. Ich wollte auch zeigen, wo wir angefangen haben. Hier haben wir mit allen Zutaten mit der anfänglichen Wasseraktivität und dem anfänglichen Feuchtigkeitsgehalt begonnen, basierend auf der Isotherme und den Massenverhältnissen. Nachdem wir alles eingegeben haben, sehen Sie, dass wir eine endgültige Wasseraktivität von 0,349 erhalten haben.
Wichtig dabei ist, dass wir mathematisch vorgehen, also wollen wir sicherstellen, dass wir eine gute Darstellung, eine gute mathematische Gleichung und Koeffizienten für jede unserer Zutaten haben. Als wir das hatten, erhielten wir unsere Vorhersage, die ziemlich genau war, und ich war damit sehr zufrieden. Die Partikelgröße bei Gewürzen, die vielleicht nicht so gut in Kontakt kommen, könnte dazu geführt haben, dass wir ein etwas anderes Ergebnis erhalten hätten, wenn wir sie länger zusammen gelassen hätten. Aber ich war mit dem Ergebnis, das wir erzielt haben, sehr zufrieden. Ich wollte dies auch nutzen, um es aus einer anderen Perspektive zu betrachten.
Wir haben die Isotherme so modelliert, wie ich sie hier in der roten Kurve zeige, aber dann wollte ich das auch mit der tatsächlichen Isotherme vergleichen, denn nachdem wir diese Mischung hergestellt hatten, haben wir tatsächlich eine Isotherme daran durchgeführt, um zu sehen, was wir damit machen können. Daraus können Sie die Unterschiede zwischen der tatsächlichen Isotherme und der modellierten Isotherme erkennen, und sie stimmen sehr, sehr gut überein, insbesondere in dem Bereich, der für uns von Interesse ist. Wenn wir nach Gewürzen suchen, vielleicht 0,2 bis 0,4, dann liegen diese im Allgemeinen im Bereich der Wasseraktivität. Sie werden feststellen, dass wir eine wirklich gute Übereinstimmung haben. Ich bin sehr, sehr zufrieden mit den Daten unserer Studie. Wie ich bereits sagte, ist dies der schlimmste Fall, den wir hatten. Die übrigen Fälle hatten tatsächlich viel bessere Ergebnisse.
Zachary:
Ich möchte einen Schritt zurücktreten und über die praktische Anwendung dieses Verfahrens nachdenken. Ich spreche ständig mit Wissenschaftlern, die unter großem Druck stehen, neue Produkte so schnell wie möglich auf den Markt zu bringen. Wenn man diese Art der Modellierung für eine Trockenzutatenmischung verwendet, erhält man auf schnelle Weise viele Erkenntnisse über das Endprodukt, noch bevor man es herstellt. Es dauert zwar ein wenig, eine Bibliothek aufzubauen und Isothermen für jede Zutat zu erstellen, aber sobald Sie das getan haben, können Sie sich an Ihren Computer setzen und sehr schnell verstehen, wie die Gleichgewichtswasseraktivität aussehen wird. Mit unserem neuen Programm im Moisture Analysis Toolkit, das mit unserem Dampfabsorptionsanalysator geliefert wird, übernimmt die Toolkit-Software die gesamte Arbeit für Sie. Sie haben diese Gleichungen erwähnt, und es gibt Gleichungen im Hintergrund, aber anstatt Ihre eigene Tabelle zu erstellen oder all dies selbst zu tun, wird all diese Arbeit für Sie erledigt, und es ist einfach, die Gleichgewichtswasseraktivität zu ermitteln.
Jetzt können Sie auch die Koeffizienten für das von Ihnen erwähnte Modell erhalten. Anhand dieser Koeffizienten können Sie Fragen stellen wie: Wie lange ist die voraussichtliche Haltbarkeit? Wie lange dauert es, bis eine kritische Wasseraktivität erreicht ist? Welche Art von Verpackung sollte ich verwenden? Wenn Sie sich die Zeit nehmen, diese Isothermen zu betrachten und genau zu verstehen, wie Sie diese Daten zur Beantwortung vieler verschiedener Fragen nutzen können, stehen Ihnen zahlreiche Möglichkeiten offen. Ich möchte nur darauf hinweisen, dass die von Ihnen gezeigten Grafiken aus der Software „Moisture Analysis Toolkit” stammen. Viele unserer Kunden, egal ob sie Nahrungsergänzungsmittel herstellen oder mit einigen der größten Gewürzproduzenten des Landes zusammenarbeiten, nutzen diese Gleichungen und Tools, um ihre Produktion zu beschleunigen.
Mary:
Guter Punkt. Ich möchte noch hinzufügen, dass ich diese Vorhersage, sobald ich die Isothermen habe, immer wieder neu durchführen kann. Ich kann jeden Teil davon ändern und innerhalb weniger Augenblicke neu ausführen. Ich könnte beispielsweise das Massenverhältnis ändern, wenn wir feststellen, dass uns diese Mischung nicht besonders gefällt oder wir die Fließfähigkeit nicht mögen oder vielleicht der Geschmack nicht gut ist. Vielleicht enthält sie zu viel Kreuzkümmel oder etwas anderes. Man könnte dieses Rezept anpassen, und das geht ganz einfach in der Software. Oder nehmen wir als Beispiel an, wir haben in früheren Webinaren über die Saisonalität gesprochen, wie diese Ihre eingehenden Zutaten verändern kann.
Die Wasseraktivität ist im Sommer tendenziell höher und im Winter niedriger. Es ist wichtig, zu überwachen, was Sie erhalten, wenn die Lieferung eintrifft, damit Sie keine Überraschungen erleben und keine Feuchtigkeit in Ihr Produkt gelangt, die Sie nicht erwartet haben oder nicht wünschen. Das können Sie hier ändern. Sie können die anfängliche Wasseraktivität jedes dieser Produkte ändern und dann einfach die Vorhersage erneut durchführen. Sobald Sie diese Informationen haben, können Sie viel damit anfangen.
Zachary:
Nun, das bezog sich hauptsächlich auf die physikalische Stabilität. Kommen wir nun zur chemischen Stabilität und sprechen wir darüber, wie wir die Wasseraktivität nutzen können, um die chemische Stabilität besser zu verstehen.
Charakterisierung der chemischen Stabilität von Pulvern
Zachary:
Um nun zur chemischen Stabilität zu kommen, möchte ich noch einmal auf unser Stabilitätsdiagramm zurückkommen, das wir zuvor gezeigt haben.
Das ist deshalb wichtig, weil Sie darüber nachdenken müssen, ob Ihr Pulver die versprochenen gesundheitlichen Vorteile bietet. Sind die Vitamine enthalten, die Sie versprochen haben, oder hat es eine chemische Veränderung gegeben, die Sie beachten müssen? Wenn Sie sich das Stabilitätsdiagramm ansehen, gibt es verschiedene Punkte in diesem Diagramm, an denen sich die Abbaurate oder die Reaktionsrate ändern wird, beispielsweise bei einer Wasseraktivität von etwa 0,6, wo es zu einer Zunahme der Bräunungsreaktionen kommen kann. Bei sehr niedrigen Wasseraktivitäten beginnt die Lipidoxidation zuzunehmen.
Sie müssen sich nur bewusst sein, wie die Wasseraktivität die Reaktionsgeschwindigkeit beeinflusst und welche Reaktionen mit dem Ende der Haltbarkeitsdauer zusammenhängen. Ich weiß, dass Sie kürzlich an einem Vitamin-C-Experiment gearbeitet haben und untersucht haben, wie es mit dieser Aktivität zusammenhängt. Können Sie dieses Experiment und Ihre Ergebnisse erläutern?
Mary:
Chemische Reaktionsgeschwindigkeiten sind etwas schwieriger zu verfolgen, aber wenn man sie verfolgen kann, ist das machbar. Um die Reaktionsgeschwindigkeiten verfolgen zu können, können wir diese Informationen nutzen, um eine Haltbarkeitsdauer und einen Zeitrahmen vorherzusagen, wann sie einen Punkt erreichen, an dem wir die Haltbarkeitsdauer als beendet betrachten würden. Unsere Studie befasste sich mit Ascorbinsäure, die wir zwei verschiedenen Wasseraktivitäten und drei verschiedenen Temperaturen aussetzten. Anschließend verfolgten wir ihren Abbau mit UV-Vis und konnten so die Geschwindigkeiten berechnen.
Einer der entscheidenden Aspekte dabei ist, dass wir die Arrhenius-Gleichung verwendet haben, die für diese Art von Reaktion sehr häufig verwendet wird. Im Grunde genommen verbindet man eine Geschwindigkeit mit einer Temperatur und einer Energie. Wir wissen bereits, dass wir Energie speziell mit der Wasseraktivität in Verbindung bringen können.
Wir führen eine Studie durch, bei der wir bei Zeitpunkt Null beginnen und dann über einen Zeitraum von mehreren Tagen bis Wochen diese Ascorbinsäure einer bestimmten Umgebung und Temperatur aussetzen, um anschließend die Veränderungen zu beobachten und grafisch darzustellen. Das ist unsere Studie. Im Wesentlichen möchten wir wissen, wie sich Temperatur und Wasseraktivität auf die Abbaurate auswirken. Wir haben hier diese Zeitdiagramme, die wir in der Grafik zeigen. Wir haben unsere Wasseraktivitäten bei 0,76 und 0,948 und die von uns verwendeten Temperaturen, und wir führen diese als beschleunigte Studie durch. Wir haben 30 °C, 40 °C und 50 °C. Im Wesentlichen geben wir dies in den Rechner ein und verwenden die Arrhenius-Gleichung, um die Informationen zu zeichnen und alles zu korrelieren. Sobald wir alle unsere Daten und unsere Studiendaten eingegeben haben, können wir dem Programm genau mitteilen, woran wir interessiert sind.
Welche Temperatur interessiert uns? Welche Wasseraktivität interessiert uns? Dann müssen wir in der Studie auch definieren, wo wir die Haltbarkeitsdauer beenden wollen. Wie viel Prozent sind noch übrig? In unserem Fall haben wir beschlossen, dass 75 % des verbleibenden Vitamin C das Ende darstellen. Wir würden also im Wesentlichen 25 % unseres Vitamin C verlieren, und dann würden wir das als Ende der Haltbarkeitsdauer bezeichnen. Wenn Sie ein Formulierer oder Hersteller sind und ein Vitamin wie das von Ihnen erwähnte haben, dann geben Sie Angaben zur Vitaminmenge oder zur Wirksamkeit Ihres Produkts. Sie würden die Haltbarkeitsdauer auf diesen Wert stützen.
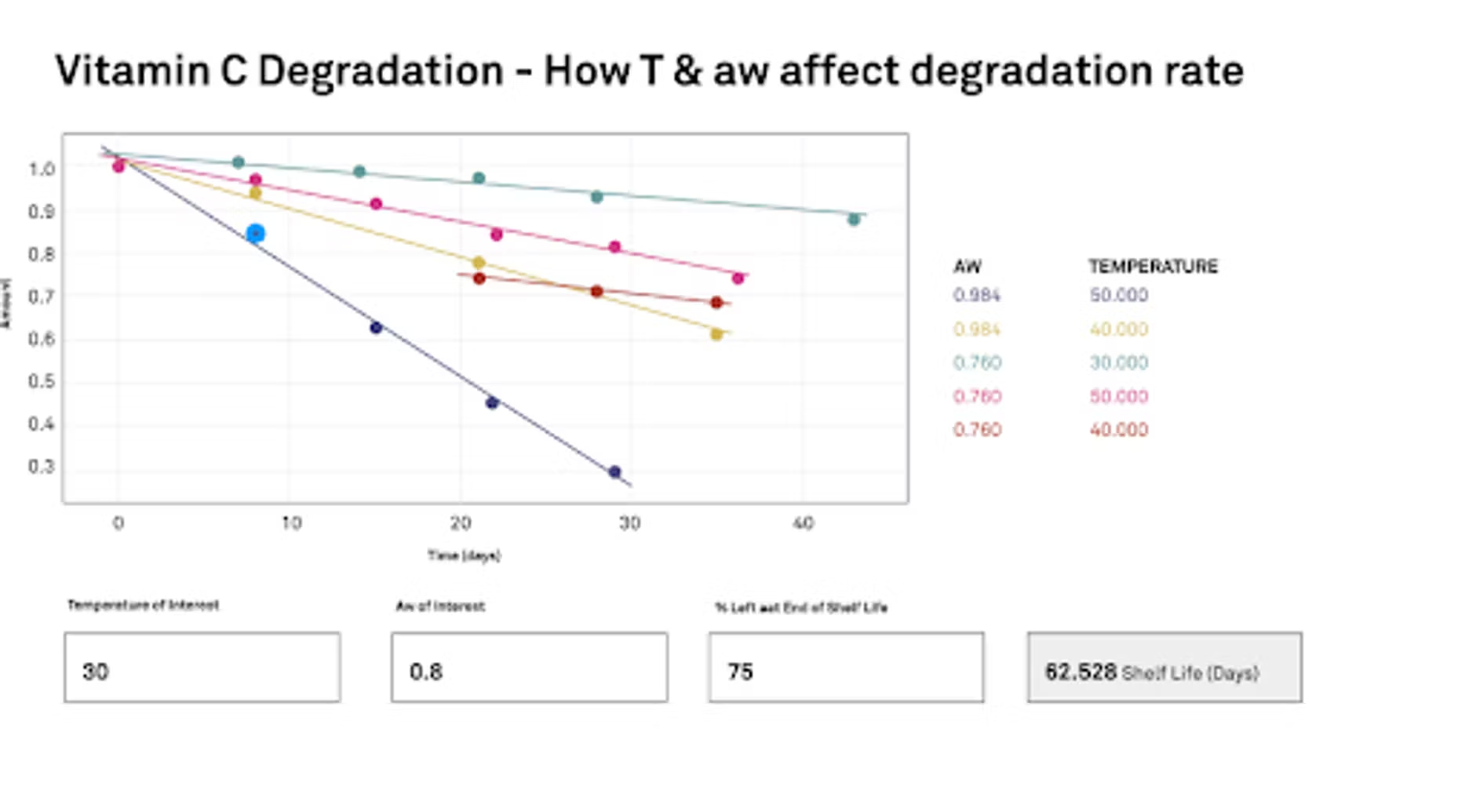
Sobald wir alle diese Informationen eingegeben haben, kann das Programm die Haltbarkeit berechnen. In unserem Fall mit Ascorbinsäure interessieren uns 30 °C und eine Wasseraktivität von etwa 0,8, was ziemlich hoch ist, aber in einem dampfenden Badezimmer durchaus möglich ist. Das entspricht einer relativen Luftfeuchtigkeit von etwa 80 %. Wie ich bereits sagte, sind 75 % das Maximum. Wir hätten 62 Tage Zeit, bevor diese Ascorbinsäure nicht mehr wirksam genug wäre.
So funktioniert chemische Stabilität im Grunde genommen. Wir müssen sie nur verfolgen, und wenn Sie in der Lage sind, sie zu messen, dann können Sie diese Studie durchführen.
Zachary:
Auch dies ist ein weiteres Tool aus dem Moisture Analysis Toolkit, das speziell für die chemische Stabilität entwickelt wurde. Auch wenn die Datenerfassung einige Zeit in Anspruch nehmen kann, lassen sich die Daten nach ihrer Erfassung ganz einfach im Toolkit grafisch darstellen. Sie haben gerade gezeigt, dass Sie eine Anfangs-Wasseraktivität und eine Temperatur von Interesse eingeben und dann definieren können, was Ihre Haltbarkeitsdauer beendet, um schnell Berechnungen zu erhalten. Auch wenn die Einrichtung einer Studie einige Zeit in Anspruch nehmen kann und es sich um Studien handelt, die wir durchführen oder bei denen wir Kunden auch durch die Verwendung von Feuchtigkeitskammern begleiten können, bieten die Berechnungen nach der Datenerfassung viel Flexibilität und liefern zahlreiche Erkenntnisse. In Ihrem Fall haben wir uns speziell mit Vitamin C befasst, aber dies könnte für alles gelten, was wir messen können, alles, dem wir einen Wert zuweisen können.
Mary:
Das funktioniert in beide Richtungen. In diesem Fall könnte es sich um die Abbaurate handeln, aber man könnte auch eine Zunahme von etwas wie einer Bräunungsreaktion oder ähnlichem im Laufe der Zeit betrachten, und das wäre dann das Ende der Haltbarkeitsdauer. Es könnte sich um einen bestimmten Farbwert handeln. Das spielt keine Rolle, solange man es messen kann. Wenn es eine Möglichkeit gibt, diese Veränderung tatsächlich zu verfolgen, kann man sie in eine Rate umwandeln und erhält dann Diagramme wie dieses.
Zachary:
Es gibt mittlerweile so viele Nahrungsergänzungsmittel und so viele Produkte in Pulverform, dass die Verwendung eines solchen Tools ihnen helfen könnte, zu verstehen, was ihr Zielwert für die Wasseraktivität ist, wie die Haltbarkeitsbedingungen aussehen oder was die Haltbarkeit beeinträchtigt. Wie viel Prozent eines bestimmten Vitamins gehen verloren und wie können sie diese Angabe auf ihrem Etikett machen? Woher wissen sie das so genau? Dies ist eine gute Methode, um das zu erreichen.
Mary:
Auch hier gilt: Sie können Ihre Interessen ändern, Sie können Ihre Interessen ändern. Sie können die Temperatur und die Wasseraktivität Ihrer Interessen ändern oder sogar, wie viel Sie am Ende möchten. All das lässt sich ganz einfach ändern, und Sie müssen nur die Vorhersage erneut ausführen.
Charakterisierung der mikrobiellen Stabilität von Pulvern
Zachary:
Schließlich die mikrobielle Stabilität. Viele Pulver haben eine geringe Wasseraktivität, und manchmal wird nicht erkannt, dass dies dennoch ein Sicherheitsrisiko darstellen kann. Ich meine, Pulver können bedenkliche Mikroorganismen enthalten, und sie mögen zwar sicher sein, aber sie sind nicht unbedingt steril. Sobald man ein Pulver rehydriert, können bei Vorhandensein von Sporen oder bedenklichen Mikroorganismen Sicherheitsprobleme auftreten. Ich habe gehört, dass Sie kürzlich an einem Artikel mitgewirkt haben, und würde mich freuen, wenn Sie etwas über den Inhalt dieses Artikels erzählen könnten.
Mary:
Sie haben es genau auf den Punkt gebracht. Es gibt die Vorstellung, dass man sich bei Lebensmitteln mit geringem Feuchtigkeitsgehalt keine Sorgen um mikrobielles Wachstum machen muss und nichts über die Wasseraktivität wissen muss, aber leider gab es viele Rückrufaktionen für Lebensmittel mit geringem Feuchtigkeitsgehalt, bei denen es zu Ausbrüchen von E. coli und Salmonellen gekommen ist, wie beispielsweise bei Erdnussbutter oder Mehl, Babybrei und ähnlichen Produkten. Das ist entmutigend. Genau das ist der Fall: Die Wasseraktivität ist eine hervorragende Möglichkeit, das Wachstum von Mikroorganismen zu begrenzen. Bei einer Wasseraktivität unter 0,6 wächst nichts. Das vermittelt ein falsches Gefühl der Sicherheit. Mein Produkt hat einen niedrigen Wert, ich muss mir keine Sorgen machen, aber die Wasseraktivität ist kein Abtötungsschritt, wie Sie gerade gesagt haben, was bedeutet, dass sie noch leben, sie befinden sich nur in einer Stasis.
Wenn sie einer höheren Luftfeuchtigkeit oder einer höheren Wasseraktivität ausgesetzt sind, wenn Sie Mehl in Keksteig geben, was Sie ja tun möchten, dann haben Sie eine Umgebung geschaffen, in der diese Mikroorganismen nun wachsen und sich vermehren können, und Sie können sehen, wo Salmonellen oder E. coli oder was auch immer für die Öffentlichkeit gefährlich werden. Das ist eigentlich ein großes Thema. Als ich kürzlich an einer Konferenz zum Thema Lebensmittelsicherheit teilnahm, wurde dies ausführlich diskutiert, es gab viele Vorträge dazu, und derzeit gibt es auch zahlreiche Forschungsarbeiten darüber, wie man diese Lebensmittel mit geringem Feuchtigkeitsgehalt sterilisieren oder pasteurisieren kann. Die Forschung wird durchgeführt, und wir kennen mehrere Forscher, und ich weiß, dass Sie das auch tun, die sehr aktiv daran arbeiten, Wege zu finden, wie wir das Wachstum von Mikroorganismen oder diese Ausbrüche verhindern können, indem wir diese Lebensmittel mit geringem Feuchtigkeitsgehalt pasteurisieren oder sterilisieren.
Zachary:
Eine dieser Forscherinnen, mit der wir kürzlich gesprochen haben, ist Dr. Jennifer Acuff. Sie untersucht Lebensmittel mit geringem Feuchtigkeitsgehalt und die Umgebungen, in denen sie hergestellt werden, und denkt über verschiedene Möglichkeiten oder Hygienetechniken nach, wie wir verhindern können, dass Lebensmittelpathogene selbst in Lebensmitteln mit geringem Feuchtigkeitsgehalt vorkommen. Wir haben kürzlich einen Podcast mit ihr aufgenommen, in dem sie darüber gesprochen hat. Aus meiner Sicht ist es wichtig, auf Hygiene zu achten und dafür zu sorgen, dass die Umgebung so sauber wie möglich ist. Darüber haben wir kürzlich auch mit Dr. Minto Michael von der Washington State University gesprochen, der sich mit Mikrobiologie befasst und weiß, dass es verschiedene Kombinationen von Temperatur, Zeit und Wasseraktivität gibt. Aber wie Sie bereits erwähnt haben, kann man nicht jede Art von Lebensmitteln erhitzen, da dies zu strukturellen Veränderungen führen würde.
Es gibt möglicherweise andere Methoden, wie Mikrowellen- oder Hochdruckverarbeitung oder etwas anderes, die wir in Kombination mit Überlegungen zur Wasseraktivität einsetzen können, um sicherzustellen, dass diese Lebensmittel so sicher wie möglich sind. Wenn Sie möchten, können Sie sich den Podcast mit Dr. Acuff oder Dr. Michael anhören, um mehr über Lebensmittelsicherheit zu erfahren.
Mary:
Ich habe auch darüber nachgedacht, welche Rolle die Wasseraktivität bei der Pasteurisierung tatsächlich spielt. Selbst wenn man das schafft, beispielsweise bei Beef Jerky oder ähnlichen Produkten, gibt es eine bestimmte Kombination aus Zeit, Temperatur und Feuchtigkeit, damit dies auch wirksam ist. Der andere Aspekt ist, dass man, wenn man dazu in der Lage ist, eine Umgebung schaffen muss, in der die Mikroorganismen, die man bekämpfen möchte, tatsächlich abgetötet werden. Wenn man die richtige Zeit und Temperatur einhält, aber die Luftfeuchtigkeit niedrig ist, ist die Sterilisation nicht so effektiv. All diese Faktoren spielen sicherlich eine Rolle.
Zusammenfassung und Empfehlungen
Zachary:
Zur kurzen Zusammenfassung:
- Heute haben wir uns mit Pulvern beschäftigt und versucht, sie zu definieren.
- Wir haben die physikalische, chemische und mikrobielle Stabilität untersucht.
- Wir haben über einige der AQUALAB-Produkte gesprochen, die wir verwendet haben, um zu recherchieren und uns über das zu informieren, worüber wir heute gesprochen haben.
Eine Sache, die ich hier erwähnen möchte, ist, dass wir zwar Lösungen zur Messung von Endprodukten oder Inhaltsstoffen anbieten, aber auch über eine Inline-Lösung namens SKALA Dry verfügen, die bei sprühgetrockneten Produkten sehr hilfreich sein kann.
Wenn Sie Schwierigkeiten haben, ein Produkt herzustellen, dessen Qualität unabhängig von der Temperatur und den Jahreszeiten gleichbleibend ist, kann SKALA Dry Ihnen automatisch dabei helfen, die richtige Wasseraktivität für dieses Produkt zu erreichen.
Schauen Sie sich auch den Podcast „Water In Food“ an, den wir erwähnt haben. Wir haben auch einen YouTube-Kanal. Hören Sie sich den Podcast an und abonnieren Sie ihn.
An dieser Stelle möchten wir die Diskussion eröffnen und einige Fragen entgegennehmen.
1. Gibt es eine Möglichkeit, die Hygroskopizität der Pulver, mit denen ich arbeite, zu messen oder zu verfolgen?
Zachary:
Gute Frage. Was die Hygroskopizität angeht, können wir uns die Form der Isothermenkurve ansehen. Das haben wir bereits zuvor angesprochen und können es jetzt wahrscheinlich noch einmal aufgreifen, aber Sie betrachten die Steigung der Kurven.
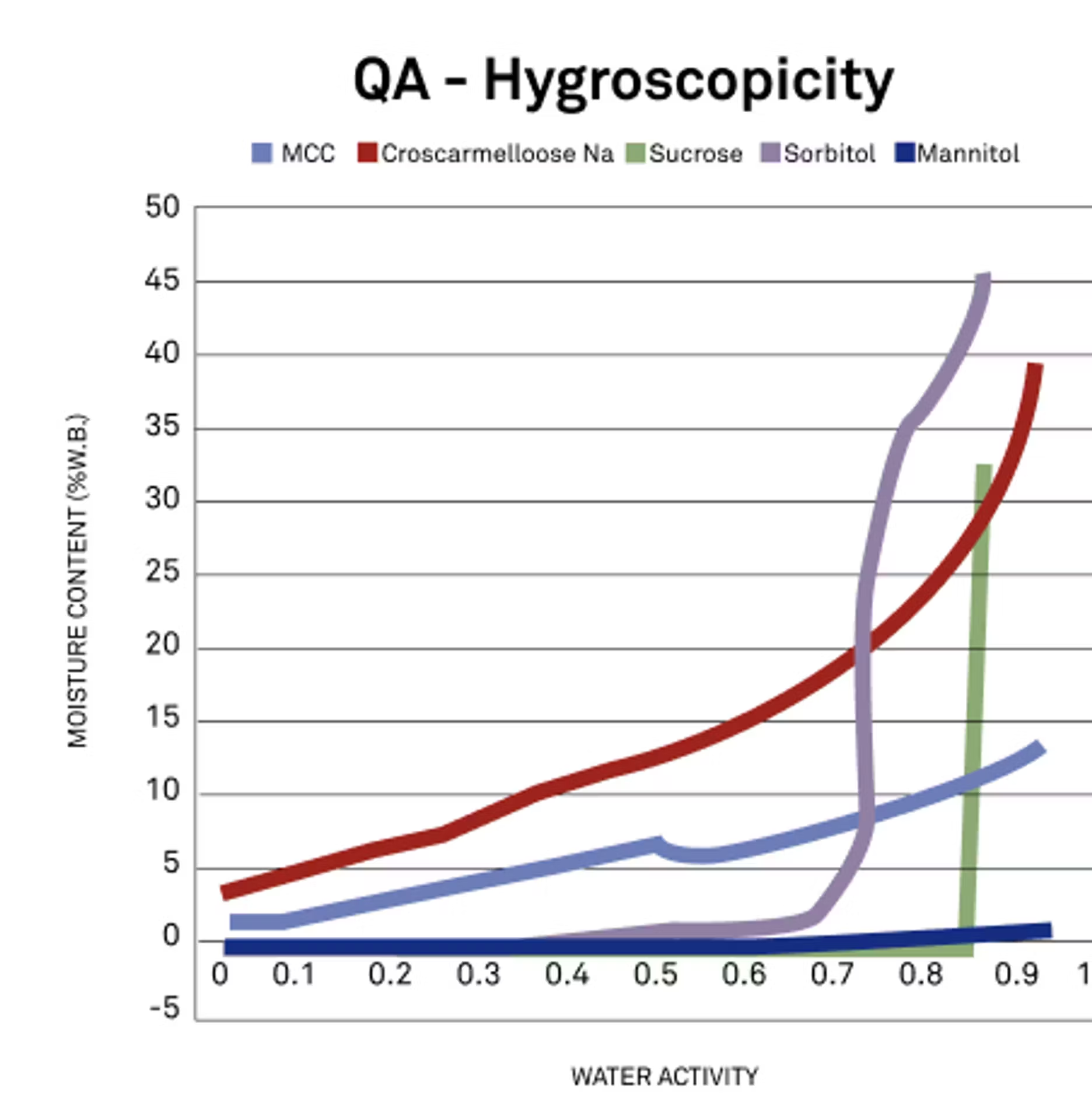
In diesem Fall betrachten wir verschiedene Hilfsstoffe, und je steiler die Kurve ist, desto höher ist die Hygroskopizität und desto mehr Wasser nimmt das jeweilige Pulver auf oder absorbiert es. Allein anhand der Form dieser Kurve können wir sehr schnell und visuell einen Unterschied in der Hygroskopizität dieser Pulver erkennen. Ich weiß nicht, ob Sie noch etwas hinzufügen möchten.
Mary:
Das ist eine gute Erklärung. Grundsätzlich gilt: Je steiler dieser Hang ist, desto hygroskopischer ist er, was auch bedeuten kann, dass er mehr Feuchtigkeit zu Ihrem Endprodukt beitragen kann, was auch immer das sein mag. Es ist auf jeden Fall wichtig, diesen Zusammenhang zu verstehen und zu wissen, wie hygroskopisch etwas ist.
Zachary:
Ich möchte noch hinzufügen, dass Sie je nach Ihrer Formel oder Ihrem Ziel oder Endergebnis möglicherweise etwas mit einer größeren Steigung wünschen oder auch nicht. Welche Art von Steigung Sie benötigen, hängt ganz vom Produkt und der Formel ab.
Mary:
Wenn Sie etwas suchen, das sich nach Belieben mit Wasser verbindet oder dessen Wassergehalt erhöht, dann ist dies eine gute Methode. Sie können eine Zutat mit einer steilen Kurve verwenden, die viel Feuchtigkeit aufnimmt und Ihrem Produkt viel Feuchtigkeit hinzufügt, und dann können Sie die Formel auf die gewünschte Wasseraktivität abstimmen. Das ist jedoch nicht unbedingt etwas Schlechtes, sondern nur etwas, das man wissen sollte.
2. Was hatte einen größeren Einfluss auf den Abbau von Vitamin C: die Temperatur oder die Wasseraktivität?
Mary:
In Ordnung, ich übernehme das. Die Wasseraktivität war definitiv der wichtigste Faktor für den Abbau von Vitamin C, mehr noch als die Temperatur. Wenn Sie sich die Daten noch einmal ansehen, können Sie das auch selbst feststellen, denn wenn Sie die Reaktionen vergleichen, bei denen nur die Temperatur variiert wurde, mit denen, bei denen wir die Wasseraktivität variiert haben, wird ganz klar, dass in diesem Fall die Wasseraktivität der wichtigere Faktor ist.
Zachary:
Das hängt von jedem einzelnen Vitamin ab, und darüber haben wir kürzlich gesprochen. Aber auch wenn Vitamin C sich auf diese bestimmte Weise verhält, muss man jedes Vitamin oder jeden Wirkstoff, der einen interessiert, einzeln betrachten. Das wird nicht immer der Fall sein. Es wird nicht immer die Wasseraktivität sein, die einen größeren Einfluss hat. Um zu verstehen, welcher Faktor den größeren Einfluss hat, muss man diese Art von Studie durchführen.
Mary:
Richtig. Denn es könnte Sauerstoff oder Vitamin E sein, das ranzig werden kann. Man könnte das nachverfolgen und hätte möglicherweise eine andere Reaktion darauf. Bei Vitamin C war es jedoch die Wasseraktivität.
3. Inwiefern hängt die Wasseraktivität oder der Feuchtigkeitsgehalt davon ab, wie schnell sich ein Pulver auflöst?
Mary:
Ich würde sagen, es geht nicht unbedingt um die Wasseraktivität oder den Feuchtigkeitsgehalt an sich, sondern eher um die Struktur des Pulvers selbst und darum, wie schnell es sich auflösen kann und in welcher Umgebung sich das Pulver befindet. Wenn es sich um ein Getränkepulver handelt, dann befindet es sich in einer Umgebung mit hoher Wasseraktivität, sodass es sich schnell auflöst. Aber das hängt davon ab. Wenn Sie beispielsweise etwas haben, das ein Hydrat enthält, ist in der Regel bereits Wasser daran gebunden, sodass es sich tendenziell schneller auflöst. Es kommt ganz darauf an. Es ist nicht so einfach, nur die Wasseraktivität und den Feuchtigkeitsgehalt eines Pulvers zu kennen, sondern es geht vielmehr um die Struktur und darum, wie schnell es sich auflösen kann.
Zachary:
Ich möchte noch hinzufügen, dass man, wenn man sich auch die Isotherme und einen DVS-Test ansieht, einen Zersetzungspunkt oder einen Punkt, an dem alles in Lösung geht, identifizieren kann. Dann können wir einen DVS-Test verwenden, um zu verstehen, wie lange dies dauern wird. Vielleicht sollte man sich die Struktur ansehen und sich auch von der Isotherme informieren lassen.
Mary:
Richtig. Ein wichtiger Aspekt bei Pulvern ist, dass sie sich auflösen lassen, denn die meisten Pulver, die wir kennen, sollen das tun. Wenn Sie nur ein Getränkepulver haben, mischen Sie es mit etwas anderem. Aber was ist, wenn Sie verhindern wollen, dass es vor dem Verpacken verklumpt und klumpt? Wir alle haben das schon erlebt, oder wir hatten schon einmal ein Getränkepulver oder etwas Ähnliches, das hart war. Vielleicht haben wir uns die Isotherme angesehen, um herauszufinden, was der kritische Punkt für diese Mischung ist, und dann dafür zu sorgen, dass wir eine Verpackung haben, die sicherstellt, dass dieser Punkt nicht überschritten wird, oder vielleicht müssen wir ein Antiklumpmittel oder etwas Ähnliches hinzufügen. All diese Faktoren beeinflussen die Löslichkeit eines Pulvers.
4. Wie ist die Haltbarkeit von amorphem Pulver im Vergleich zur Haltbarkeit von kristallinem Pulver?
Zachary:
Das hängt davon ab, was die Haltbarkeit beendet. Handelt es sich um eine Veränderung der Textur oder um eine chemische Veränderung? Zunächst müssten wir definieren, wie dieser Endpunkt aussieht, und dann überlegen, was Sie hinzufügen würden.
Mary:
Gute Frage. Kristalline Pulver haben einen Zersetzungspunkt, den ich bereits erwähnt habe. Ich weiß, dass sie von einem festen in einen flüssigen Zustand übergehen, und das hängt von der Luftfeuchtigkeit ab, der sie ausgesetzt sind. Wenn man die Umgebung um dieses kristalline Pulver herum unter diesem Punkt halten kann, dann kann es seine Aktivität schnell verändern, ohne dass sich die Struktur des Pulvers verändert. Man kann eine wirklich lange Haltbarkeit erreichen. Man kann sich das wie bei Saccharose oder NACL oder ähnlichen Stoffen vorstellen. Man hat einfach eine lange Haltbarkeit damit.
Aber wenn es darüber liegt, dann haben Sie ein Problem. Es kommt doch auf alles an, anders als Sie gesagt haben: Was beeinflusst die Haltbarkeit? In welcher Umgebung wird es verwendet? Was ist dann sinnvoll? Wir haben auch ein Webinar über Süßstoffe veranstaltet, und das war ein interessanter Teil über Süßstoffe und ihre Eigenschaften hinsichtlich ihrer Löslichkeit, und wir wechseln zwischen amorphen und kristallinen Strukturen, und wie das im Wesentlichen aus einem Produkt heraus ausfallen könnte, ist eine komplizierte Frage. Gibt es eine eindeutige Antwort? Vielleicht versuche ich es einfach zu vereinfachen. Kristalline Strukturen: Wenn man sie unterhalb des kritischen Punktes halten kann, kann man sie allem aussetzen, was darunter liegt. Es wird sich wirklich nichts ändern, da jede Wasserinteraktion wie eine Oberfläche ist. Aber wenn es darüber liegt oder wenn es sich um eine chemische Reaktion oder etwas anderes handelt, dann ist das eine andere Sache, über die wir sprechen müssen.
Zachary:
Ich möchte nur hinzufügen, dass bei kristallinen Feststoffen oder Pulvern die Delikueszenzpunkte in der Regel recht hoch sind, vielleicht bei einer Wasseraktivität von 0,9 oder irgendwo in diesem Bereich, während ein amorphes Pulver bei einer Wasseraktivität von 0,3 bis 0,6 eine physikalische Veränderung erfahren kann. Wenn es allein um die Textur geht, die die Haltbarkeit bestimmt, dann würde ich mir vorstellen, dass die meisten kristallinen Feststoffe eine längere Haltbarkeit haben. Wenn es jedoch um chemische Stabilität oder chemische Reaktionen geht, sind tiefgreifendere Untersuchungen und Experimente erforderlich, um diese Frage zu beantworten.
Mary:
Was wir noch nicht erwähnt haben, ist, dass kleine Partikelgrößen, ungewöhnliche Strukturen oder Formen oder unterschiedliche Größen einen Einfluss darauf haben können, wo bei Raumfeuchtigkeit überraschend Brückenbildung auftritt. Selbst wenn man sagt, dass Kristalle unterhalb des Zersetzungspunktes stabil sind, hat die Partikelgröße definitiv einen Einfluss auf die Stabilität der Kristallstruktur.
Newsletter-Anmeldung
Fallstudien, Webinare und Artikel, die Ihnen gefallen werden.
Erhalten Sie regelmäßig die neuesten Inhalte!
