Webinar
Attività acquatica 101: Padroneggia le basi
Una solida comprensione dell'attività dell'acqua ti dà la possibilità di migliorare notevolmente il tuo prodotto, il suo imballaggio e il modo in cui lo produci. Cominciamo dalle basi.

Comprendere il potere dell'attività dell'acqua
L'attività dell'acqua non è un concetto intuitivo per la maggior parte delle persone. Ma una volta compreso, può dare il potere di controllare l'umidità negli alimenti. Prevenire la crescita microbica è solo l'inizio.
Scopri gli aspetti fondamentali delle attività acquatiche condensati in questo webinar di 20 minuti. Imparerai:
- Che cos'è l'attività dell'acqua
- In che cosa differisce dal contenuto di umidità
- Perché controlla la crescita microbica
- Come comprendere l'attività dell'acqua può aiutarti a controllare l'umidità nel tuo prodotto.
Presentatore
Mary Galloway è stata per otto anni ricercatrice capo presso il laboratorio di ricerca e sviluppo di AQUALAB. È specializzata nell'uso e nella verifica di strumenti che misurano l'attività dell'acqua e la sua influenza sulle proprietà fisiche. Ha collaborato con numerosi clienti per risolvere i loro problemi relativi all'umidità dei prodotti e spesso le viene chiesto: "Che cos'è l'attività dell'acqua?".
Attività dell'acqua 101
In che modo i produttori alimentari mantengono la consistenza morbida dell'uvetta e croccante dei fiocchi di avena, evitano la formazione di grumi e agglomerati o determinano se un prodotto è soggetto a deterioramento? Tutti questi aspetti sono controllati dall'attività dell'acqua. Comprendendo il funzionamento dell'attività dell'acqua, è possibile sviluppare prodotti appetibili e prevedere e prevenire potenziali problemi di conservazione.
Attività dell'acqua definita
Principi della termodinamica:
- L'energia è una forza motrice che permette ai processi di avvenire.
- Più energia significa che è possibile eseguire più processi o lavori (ad esempio meccanici, termici, chimici).
- Uno stato ad alta energia vuole convertirsi in uno stato a energia più bassa per diventare più stabile.
L'attività dell'acqua (aw) è la misura dello stato energetico dell'acqua in un sistema. È un principio della termodinamica e segue le stesse regole. Un'attività dell'acqua più elevata significa più energia e l'acqua può svolgere più lavoro, come la crescita microbica, la migrazione dell'umidità o le reazioni chimiche e fisiche. Le differenze nell'attività dell'acqua determineranno il modo in cui l'umidità si muove (in termini di energia, non di concentrazione). L'acqua con un'attività dell'acqua più elevata ha più energia rispetto all'acqua con un'attività dell'acqua più bassa. In che modo l'acqua abbasserà il suo stato energetico per diventare più stabile? Migrerà verso un'attività dell'acqua più bassa.
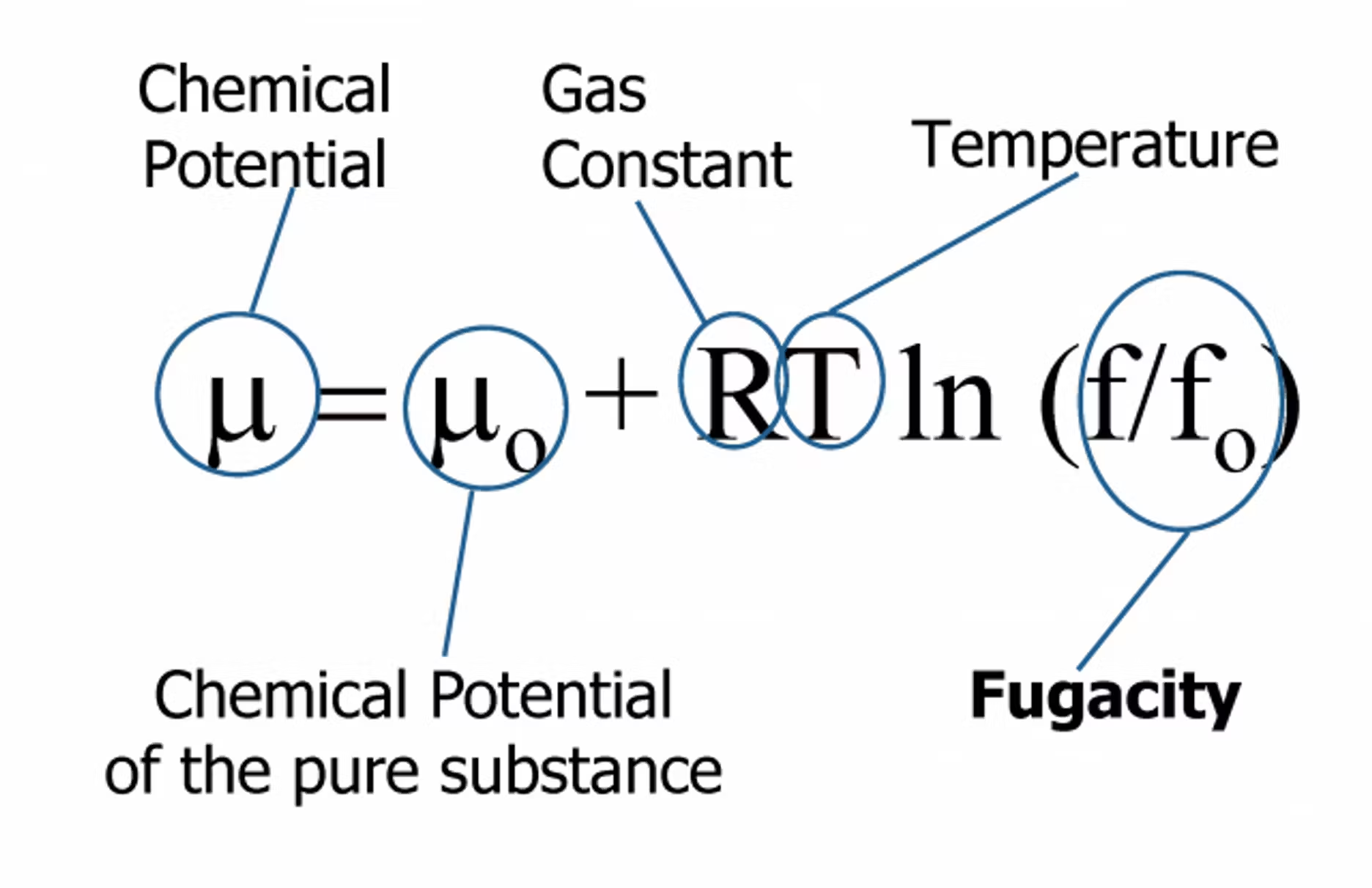
Nei sistemi energetici, possiamo adattare l'equazione dell'energia libera di Gibbs (Equazione 1) per determinare l'attività dell'acqua in un sistema a una data temperatura. L'energia dell'acqua in un sistema è uguale all'energia dell'acqua pura (𝜇o) più la costante dei gas (R) moltiplicata per la costante della temperatura (T) e il logaritmo naturale della fugacità. Si noti che l'unica variabile dipendente in questa equazione per determinare l'energia dell'acqua è la fugacità.
Che cos'è la fugacità?
La fugacità (f/f0) è la tendenza di un materiale a disperdersi o la quantità di vapore che può fuoriuscire da un campione.
- f/f0 = p/p0
- p/p0 = Pressione di vapore dell'acqua sopra il campione a 𝓧 °C / Pressione di vapore dell'acqua pura a 𝓧 °C
- p/p0 = aw
La fugacità si misura in base alle pressioni parziali, ovvero la pressione di vapore dell'acqua sopra un campione a una temperatura specifica, divisa per la pressione di vapore dell'acqua pura alla stessa temperatura. E la pressione di vapore relativa (talvolta chiamata pressione di vapore parziale) è esattamente l'attività dell'acqua. Quindi, se determiniamo la pressione di vapore parziale di un campione, possiamo calcolare l'attività dell'acqua.
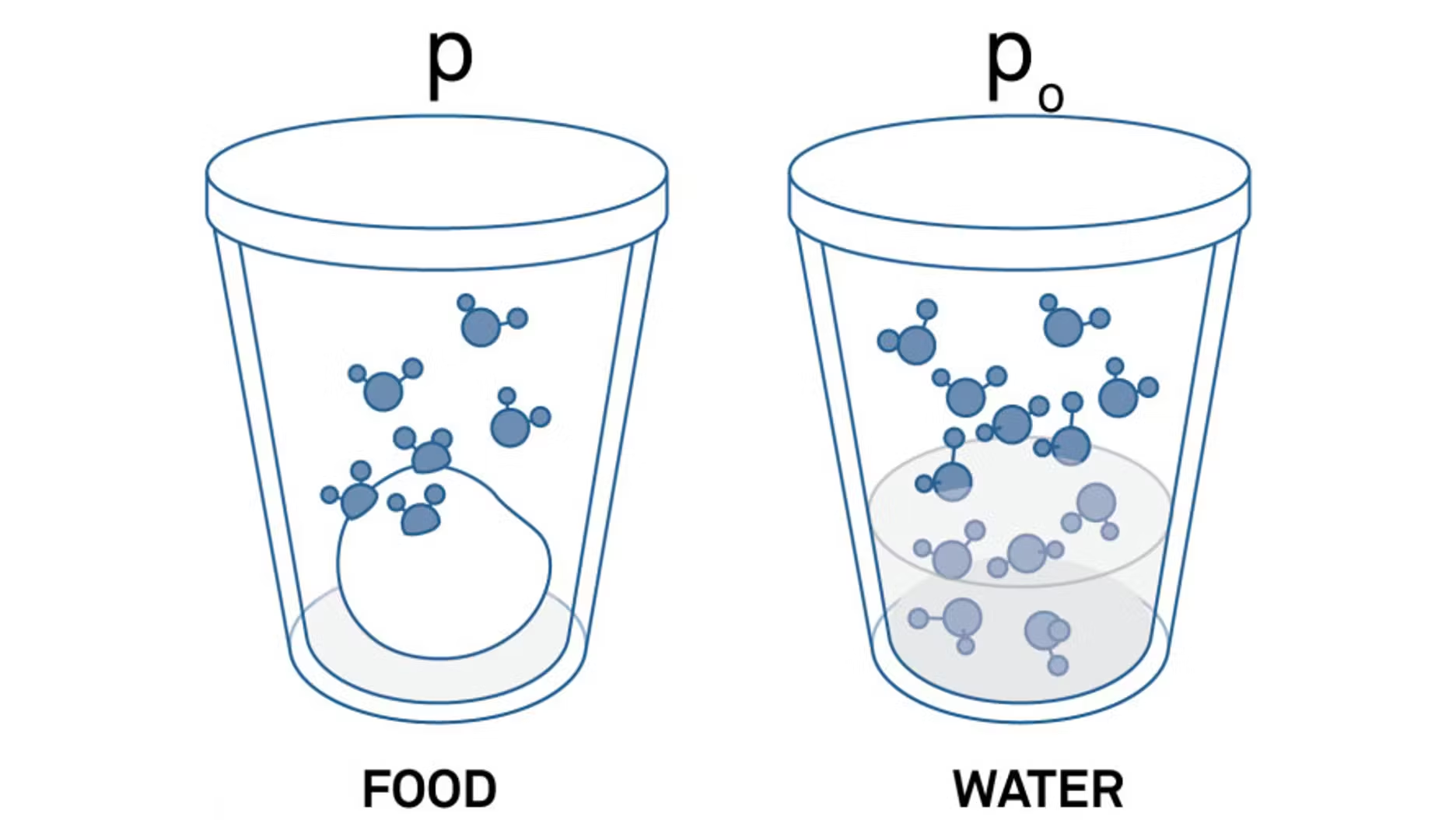
La figura 1 illustra cos'è la pressione di vapore. A sinistra è presente un campione di alimento in un contenitore. Le molecole d'acqua fuoriescono dal campione e si disperdono nello spazio di testa. Queste molecole producono una pressione specifica all'interno del contenitore sigillato. Questa pressione viene confrontata con la pressione prodotta dall'acqua pura, come dimostrato nel contenitore a destra. Poiché l'attività dell'acqua è un rapporto tra due pressioni, è priva di unità di misura e viene misurata su una scala da 0 (nessuna energia) a 1 (la stessa energia dell'acqua pura).
È importante sottolineare che la pressione deve essere lasciata equilibrare e che la temperatura e la pressione devono essere costanti. L'attività dell'acqua a 25 °C sarà diversa dall'attività dell'acqua a 35 °C. In genere, sarà più alta. Quindi, se un giorno si effettua una lettura a 25 °C e il giorno successivo la si effettua a una temperatura diversa, l'attività dell'acqua non sarà la stessa, poiché l'attività dell'acqua dipende dalla costanza della temperatura.
Contenuto di umidità definito
Metodo primario: perdita all'essiccamento (Equazione 2)

Metodo primario: Titolazione (Equazione 3)
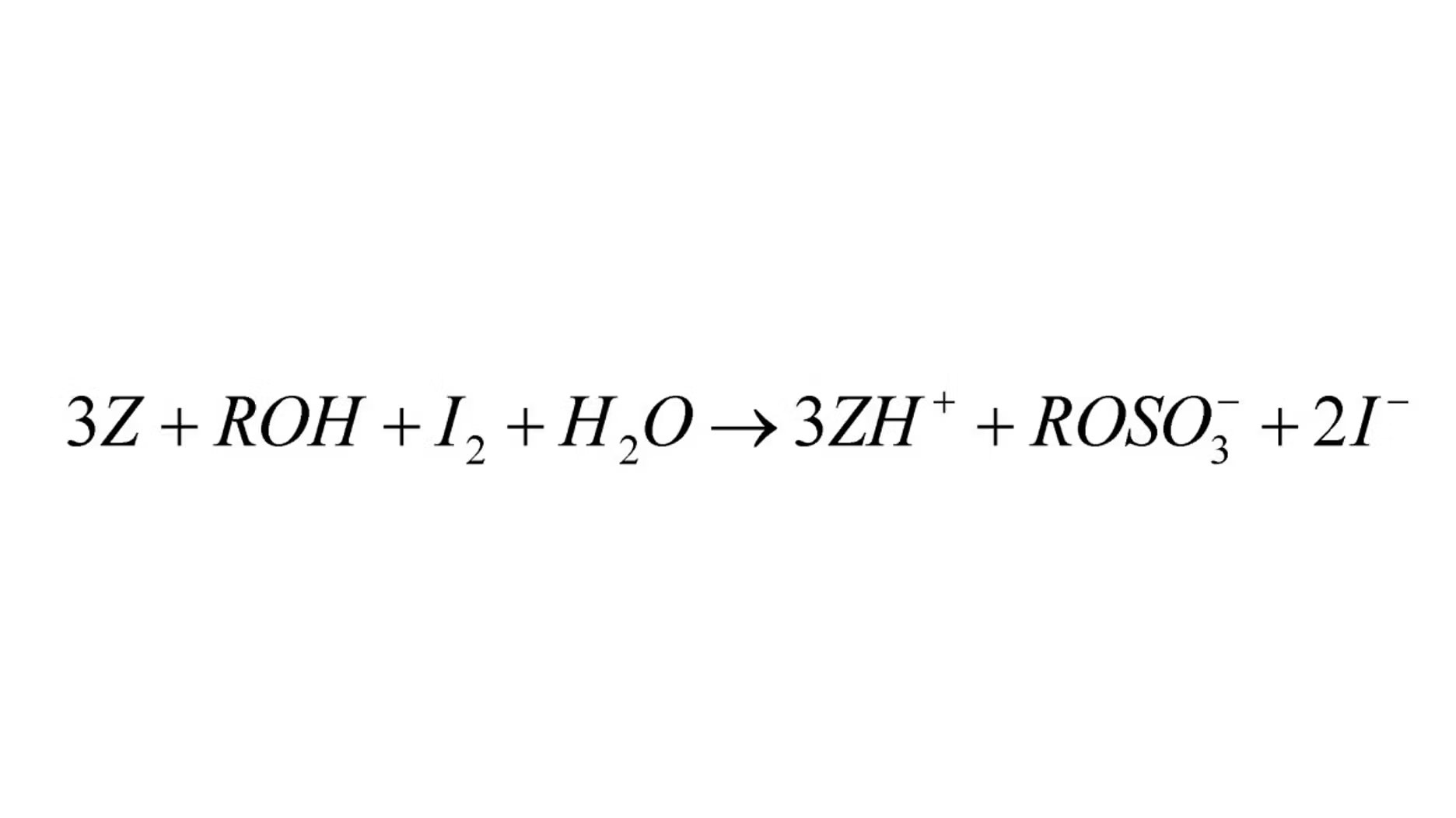
A differenza dell'attività dell'acqua, che è uno stato energetico, il contenuto di umidità è una misura qualitativa, ovvero una quantità, di acqua. Non è una forza motrice. Influisce sulla consistenza, ma non è una forza motrice per le reazioni o i cambiamenti in un prodotto. Esistono due metodi principali utilizzati per misurarlo.
Perdita per essiccamento: la perdita per essiccamento prende il peso umido di un campione e sottrae il peso secco, quindi divide per il peso secco per la base secca o per il peso umido per la base umida, quindi moltiplica il totale per 100 per ottenere una percentuale. È importante sapere quale base viene utilizzata perché ciascuna fornisce un risultato diverso. Questo perché si divide per pesi diversi. Purtroppo, la base non viene spesso indicata nella perdita per essiccamento. Di solito viene indicata solo come percentuale di contenuto di umidità. Noi di METER utilizziamo la base umida perché la base secca può dare un contenuto di umidità negativo, che non è reale. Un altro problema della perdita per essiccazione è che sostanze diverse dall'acqua, come alcoli e altri volatili, possono evaporare, aumentando il contenuto di umidità.
Titolazione: (nota anche come Karl Fischer) Si tratta di una reazione chimica che utilizza acqua, iodio e alcuni solventi. La reazione continua fino a quando tutta l'acqua è stata consumata, a quel punto la conduttività elettrica nella soluzione cambia. La conduttività viene misurata e quindi utilizzata per calcolare la percentuale di umidità. Questo metodo presenta alcuni potenziali problemi, uno dei quali è che tutta l'acqua deve essere solubilizzata e disponibile per reagire, il che può essere difficile se il prodotto non è liquido. Per poterlo fare è necessario sapere quale solvente utilizzare, e non esiste un solvente valido per tutti i casi. Esiste un solvente principale che funziona con molti tipi di campioni, ma non è efficace per tutti i campioni. Inoltre, con i solventi possono verificarsi reazioni collaterali che possono influenzare la misurazione.
Uno dei problemi legati alla misurazione del contenuto di umidità è che non esiste uno standard. Non esiste nulla che abbia un contenuto di umidità intrinseco pari a X con cui poter effettuare un confronto. È possibile ottenere una risposta relativa alla percentuale di umidità, ma non è possibile sapere se sia accurata.
Dimostrazione dell'attività dell'acqua
Se si confronta il contenuto di umidità di un biscotto con quello del miele, ci si aspetterebbe che il contenuto di umidità del miele sia più elevato. Questo è vero: il miele ha un contenuto di umidità del 18%, mentre un biscotto ha un contenuto di umidità del 5%. Ma questi due prodotti hanno la stessa attività dell'acqua (0,60 aw), il che significa che se immergeste il biscotto nel miele per una settimana, il biscotto non diventerebbe morbido. Perché? Perché è l'attività dell'acqua, non il contenuto di umidità, la forza motrice delle reazioni (in questo caso la migrazione dell'umidità). Non accadrebbe nulla perché le energie (o le attività dell'acqua) sono le stesse.
Applicazioni per l'attività dell'acqua e il contenuto di umidità
Esistono applicazioni sia per l'attività dell'acqua che per il contenuto di umidità (Tabella 2). L'attività dell'acqua è un modo più accurato per prevedere e prevenire i problemi di conservazione, ma occorre tenere presente che il contenuto di umidità influisce sulla consistenza. È possibile utilizzare il contenuto di umidità per migliorare la consistenza, a seconda del tipo di prodotto desiderato. Può anche essere utilizzato per determinare le concentrazioni degli ingredienti o il contenuto nutrizionale, che è importante per i requisiti di etichettatura. Inoltre, se il prodotto ha un limite di contenuto di umidità, ad esempio il 10% per gli alimenti per animali domestici, è necessario determinare il contenuto di umidità per sapere se il prodotto è conforme.
Isoterme di assorbimento dell'umidità
Ogni prodotto presenta un rapporto unico tra attività dell'acqua e contenuto di umidità. La figura 2 mostra il rapporto tra attività dell'acqua e contenuto di umidità nei prodotti che abbiamo testato. Sono tutti completamente diversi e ogni grafico ha una forma diversa.

La relazione tra attività dell'acqua e contenuto di umidità è chiamata isoterma di assorbimento dell'umidità e può essere utilizzata per determinare l'attività critica dell'acqua. È qui che le proprietà di assorbimento dell'umidità cambiano fisicamente e possono assorbire più umidità. L'attività critica dell'acqua è determinata da un cambiamento nella pendenza della curva. All'attività dell'acqua in cui la pendenza cambia, il prodotto cambierà di consistenza o subirà altri tipi di reazioni.
È possibile determinare l'effetto della formulazione confrontando diverse isotermiche da una formulazione all'altra. Ad esempio, è possibile modellare la miscelazione di ingredienti secchi per prevedere l'attività dell'acqua quando si mescolano due nuovi ingredienti. È anche possibile determinare l'effetto dell'abuso di temperatura; se un prodotto viene spedito e conservato in un camion o in un magazzino caldo, cosa succederà al prodotto quando arriverà al rivenditore? È possibile eseguire isotermiche a diverse temperature e prevederne l'effetto. Le isotermiche sono essenziali anche per prevedere la durata di conservazione.
Crescita microbica
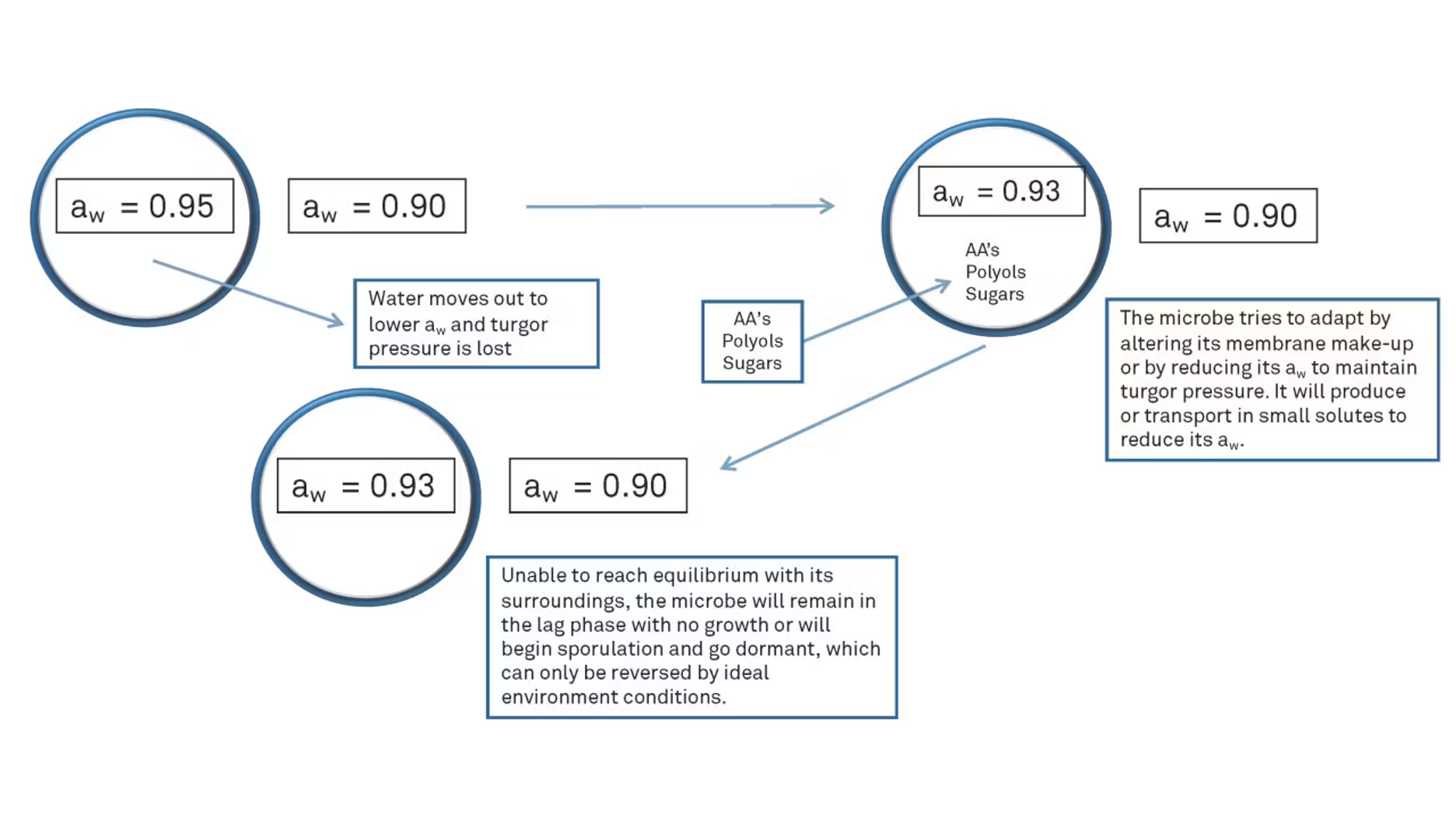
I microrganismi hanno bisogno di acqua per crescere e la ottengono dall'ambiente circostante. Quando un organismo è circondato da un'attività dell'acqua inferiore a quella interna, subisce uno stress osmotico. Nella figura 3, l'attività dell'acqua all'interno di una cellula è pari a 0,95 aw. All'esterno della cellula, l'attività dell'acqua è pari a 0,90 aw. Poiché un'attività dell'acqua elevata tende a diventare un'attività dell'acqua bassa, l'acqua all'interno della cellula tenderà a fuoriuscire e, quando ciò accadrà, la cellula perderà la pressione turgorale. La cellula cercherà di adattarsi modificando il proprio processo metabolico per ridurre l'attività dell'acqua al suo interno. Se riuscirà ad adattarsi all'ambiente, avrà acqua o energia sufficienti per crescere e riprodursi.
Ma cosa succede se non è in grado di adattarsi all'ambiente? Un'altra cellula nella Figura 3 ha un'attività dell'acqua pari a 0,93, ma non è in grado di adattarsi all'ambiente con un valore pari a 0,90. In questo caso, l'energia non è sufficiente per consentire alla cellula di crescere e riprodursi, che quindi entrerà in uno stato di dormienza.
La capacità di un microbo di adattarsi e ridurre la propria attività idrica determina il limite della sua attività idrica. Negli anni '50, il dottor William James Scott dimostrò che i microrganismi hanno un livello di attività idrica al di sotto del quale non crescono (Tabella 3). Esiste un'attività idrica specifica per ciascun microrganismo che ne inibisce la crescita, e questi non possono crescere in un ambiente al di sotto di tale limite.
La tabella 3 mostra che la salmonella ha un limite di attività dell'acqua pari a 0,95. Ciò significa che se un prodotto ha un'attività dell'acqua pari a 0,95 e le condizioni sono ideali in termini di pH, temperatura, nutrienti e non sono presenti specie concorrenti, la salmonella non può proliferare. Se una qualsiasi di queste condizioni cambia o non è ideale per la crescita microbica, l'attività dell'acqua limite potrebbe aumentare. I batteri possono crescere con un'attività dell'acqua superiore a questo limite, ma non possono mai crescere con un'attività dell'acqua inferiore. E non importa in quale matrice si trovino i batteri, che sia un biscotto, una polvere o un alimento per animali domestici, se questi batteri sono presenti, non cresceranno al di sotto di quel limite.
Si noti che l'attività dell'acqua non è una fase di eliminazione o rimozione dei batteri. Si tratta di una fase di controllo che impedisce la crescita dei microrganismi, il che significa che il prodotto è sicuro ma non sterile. I batteri sono ancora presenti. Se questi alimenti fossero esposti a un'attività dell'acqua superiore al loro limite, potrebbero crescere. Si tratta di un potenziale problema, ma se si formula il prodotto in modo da mantenere l'attività dell'acqua sufficientemente bassa, non ci saranno problemi.
La tabella 3 mostra anche che i batteri stafilococchi aerobici hanno un'attività dell'acqua minima di 0,86. Ciò significa che tutto ciò che supera 0,86 aw è considerato un alimento potenzialmente pericoloso. Se questi batteri iniziano a proliferare, provocano malattie, quindi gli alimenti con un'attività dell'acqua superiore a tale valore sono considerati potenzialmente pericolosi. Tutto ciò che è inferiore a 0,85 aw è un limite al di sotto del quale ciò non può accadere.
La tabella 4 è un grafico che mostra l'intero intervallo di attività dell'acqua per vari organismi, inclusi muffe e lieviti. Mostra anche gli alimenti tipici che si trovano in ciascun intervallo di attività dell'acqua. Si noti che al di sopra di 0,85 si trovano gli alimenti potenzialmente pericolosi. Le muffe hanno limiti di attività dell'acqua inferiori, ma quelle generalmente coinvolte nel deterioramento sono pari o superiori a 0,7. Non vi è crescita per nessun microbo al di sotto di 0,6. È possibile utilizzare queste informazioni per produrre prodotti che non siano potenzialmente pericolosi o suscettibili alle muffe di deterioramento.
L'attività dell'acqua in azione
Prevenire la muffa
Un coltivatore ha essiccato le sue noci pecan fino a raggiungere un contenuto di umidità del 4%. Non era sicuro che il 4% fosse sufficientemente secco da impedire la crescita microbica, ma storicamente non aveva mai avuto problemi con questa specifica. Se avesse esaminato un'isoterma di assorbimento dell'umidità per determinare la relazione tra attività dell'acqua e contenuto di umidità, avrebbe visto che un'attività dell'acqua di 0,68 nelle sue noci pecan corrisponde a un contenuto di umidità del 4%. 0,68 è al di sotto del limite microbico per la crescita della muffa. Quindi, se la sua attività dell'acqua rimane a 0,68, un contenuto di umidità del 4% è sufficiente per prevenire la muffa.
Ma il prodotto dell'agricoltore ha fatto la muffa. Perché?
La sua misurazione del contenuto di umidità era accurata solo allo 0,5%. Quando le noci pecan misuravano il 4%, in realtà erano più vicine al 4,5%, il che significava che l'attività dell'acqua superava il limite di sicurezza per la muffa. Il contenuto di umidità non era una specifica di qualità adeguata perché le noci pecan potevano avere un contenuto compreso tra il 3,5 e il 4,5% e il coltivatore non avrebbe mai potuto saperlo.
Se il contenuto di umidità delle noci pecan coltivate oscilla dal 3,5 al 4,5%, non solo le noci sono soggette alla muffa, ma potrebbero anche generare meno profitti. Un contenuto di umidità inferiore significa una qualità inferiore (noci più dure) e un numero maggiore di noci in ogni sacchetto (imballaggio eccessivo). Tuttavia, se avesse utilizzato una specifica di attività dell'acqua più accurata, avrebbe potuto evitare entrambi i problemi. Avrebbe potuto mantenere il contenuto di umidità esattamente al 4% utilizzando una specifica di attività dell'acqua di 0,68.
Prevedere l'agglomerazione e la formazione di grumi
Un produttore di zuppe disidratate ha lavorato una miscela fino a ottenere un contenuto di umidità del 3%. Ha ricevuto del pepe fresco da aggiungere alla miscela, anch'esso con un contenuto di umidità del 3%. Tuttavia, quando ha mescolato i due ingredienti, l'intero lotto si è aggregato. Cosa è successo? Anche se il contenuto di umidità era lo stesso, l'attività dell'acqua era diversa.
Il mix della zuppa era 0,28 aw, mentre l'attività dell'acqua del pepe era 0,69 aw, superiore all'attività critica dell'acqua della zuppa. Un'attività dell'acqua più elevata tende sempre a ridursi, quindi l'umidità è migrata dal pepe alla zuppa causando l'aggregazione della miscela. Se il produttore avesse misurato l'attività dell'acqua prima di aggiungerla alla zuppa, avrebbe potuto prevedere l'agglomerazione e la formazione di grumi, poiché sapeva che 0,69 aw era superiore al limite critico per la zuppa. Monitorando l'attività dell'acqua degli ingredienti in entrata, il produttore avrebbe potuto controllare la qualità dei propri fornitori e stabilire una specifica di accettazione inferiore all'attività dell'acqua critica. Avrebbe potuto utilizzare queste informazioni per ottenere una maggiore uniformità negli ingredienti in entrata.
Formulare per il successo
Anche l'attività dell'acqua è fondamentale nella formulazione dei prodotti. Se producessi uno snack dolciario e generassi isotermiche per la glassa, il ripieno di crema e la torta, noteresti che ogni ingrediente ha un rapporto diverso tra attività dell'acqua e contenuto di umidità. Ogni curva ha una forma diversa (Figura 4).

Con un'attività dell'acqua appena inferiore a 0,7 (linea verticale), gli ingredienti hanno tutti un contenuto di umidità diverso. La glassa è al 5%, la crema è vicina al 15% e la torta è al 20%. Ogni contenuto di umidità conferisce una consistenza diversa quando il cliente morde il dolcetto. È possibile formulare ogni ingrediente in base a questa esatta attività dell'acqua e ogni componente manterrà il proprio contenuto di umidità e la propria consistenza. Poiché l'attività dell'acqua di ogni componente è la stessa, l'umidità non migrerà da un componente all'altro.
Riduci gli imballaggi eccessivi e aumenta i profitti
Un produttore di alimenti per animali domestici ha prodotto un prodotto con un contenuto di umidità del 6,5% perché non ha mai avuto problemi di deterioramento con quella specifica. Ha creato un isotermo e ha scoperto che con un contenuto di umidità del 6,5% il suo prodotto aveva un'attività dell'acqua pari a 0,4, ben al di sotto di qualsiasi limite microbico. Ma le sue specifiche relative all'umidità erano troppo basse? Poiché per gli alimenti per animali domestici è consentito un contenuto massimo di umidità del 10%, avrebbe potuto tranquillamente aumentare il contenuto di umidità e l'attività dell'acqua per aumentare il suo margine di profitto e migliorare la consistenza.
Dopo aver utilizzato i dati isotermici per identificare un limite critico di attività dell'acqua e aver eseguito i calcoli relativi alla durata di conservazione, il produttore di alimenti per animali domestici ha fissato una nuova specifica di attività dell'acqua pari a 0,6, che corrisponde a un contenuto di umidità del 9,5%. Entrambi questi valori rientravano nei limiti di sicurezza e normativi. Aumentando l'attività dell'acqua e la specifica del contenuto di umidità, ha ridotto il costo delle materie prime. Ha utilizzato meno ingredienti per produrre la stessa quantità di alimenti per animali domestici, sostituendo essenzialmente tali ingredienti con acqua. Ha anche ridotto il consumo di elettricità e calore grazie al minor tempo di permanenza nei forni. Inoltre, il prodotto era migliore perché il contenuto di umidità era più elevato. Comprendendo l'attività dell'acqua, il produttore è stato in grado di aumentare costantemente i profitti senza compromettere la qualità o la sicurezza.
Aumentare la stabilità chimica/biochimica
L'attività dell'acqua può influenzare la velocità di reazione di vari tipi di reazioni chimiche che avvengono negli alimenti e nei prodotti farmaceutici.

La figura 5 è un grafico elaborato dal dottor Ted Labuza che mostra come la maggior parte delle velocità di reazione aumenti con attività dell'acqua vicine a 0,6. Il grafico illustra dove crescono batteri, lieviti e muffe. Mostra anche dove aumenta l'attività enzimatica. Le reazioni di imbrunimento raggiungono il picco intorno a 0,6 e poi diminuiscono perché a quel punto c'è più acqua nella matrice e vengono diluite. L'ossidazione dei lipidi segue un andamento insolito, essendo elevata a basse attività dell'acqua e di nuovo elevata a attività dell'acqua più elevate. È interessante notare che è più stabile a attività dell'acqua comprese tra 0,3 e 0,4, il che è importante per alcuni prodotti come le patatine che contengono molto grasso e olio.
Perché è necessaria l'attività dell'acqua
L'attività dell'acqua è l'energia dell'acqua in un sistema. È qualitativa e intrinseca al prodotto stesso. È una forza motrice che consente il verificarsi di fenomeni quali la crescita microbica, la migrazione dell'umidità e i cambiamenti fisici e chimici. Il contenuto di umidità è semplicemente la quantità di acqua presente. Non è una forza motrice, quindi non indica cosa farà l'acqua, ma solo quanta ce n'è.
L'attività dell'acqua è la specifica giusta per prevenire la crescita microbica, mantenere la stabilità fisica e chimica, formulare prodotti e prevedere la durata di conservazione.
Riferimenti
Labuza, Ted P., K. Acott, S. R. TatiNl, R. Y. Lee, Jv Flink e W. McCall. "Determinazione dell'attività dell'acqua: uno studio collaborativo su diversi metodi". Journal of Food Science 41, n. 4 (1976): 910-917.
Scott, W. J. "Relazioni idriche dei microrganismi responsabili del deterioramento degli alimenti". In Advances in food research, vol. 7, pagg. 83-127. Academic Press, 1957.
Iscrizione alla newsletter
Casi di studio, webinar e articoli che ti piaceranno.
Ricevi regolarmente gli ultimi contenuti!
